1.31 物質使用障害の神経科学
KHALED MOUSSAWI, M.D., PH.D.
「薬物中毒(Drug addiction)」は現在の日常語として残る可能性が高いですが、意味論的・否定的なスティグマが伴うため、医学用語としては不適切です。特に、薬物誤用が薬物中毒に分類される正確な時点を特定することは不可能です。同様に、「薬物依存(drug dependence)」も、依存が物質に対する正常な生理的反応である可能性があるため、疾患の医学用語としては不適切です。DSM-5で定義されている**物質使用障害(Substance Use Disorder: SUD)**は、DSM-IVの物質誤用と依存のカテゴリーを、軽度から重度までの連続体で測定される単一の障害として統合することで、これらの問題を解決しています。DSM-5では、各特定の物質(以下「薬物」と称する)のクラス(例:アルコール、覚せい剤)が個別に扱われ、3つの明確な薬物関連現象(SUD、物質中毒、物質離脱)に対する診断基準が提供されています。ほとんどの薬物における障害は同じ全体的な基準(表1.31-1)に基づいて診断されますが、異なる薬物への慢性的な曝露が異なる神経適応パターンを生み出すことがますます明らかになっています。
臨床的には、重度のSUDは、表1.31-1に列挙されたDSM-5基準のうち6つ以上を満たすものと定義されます。神経生物学的観点から見ると、重度のSUDは、薬物へのアクセスが妨げられた場合に生じる渇望と強迫的な薬物探索・摂取、および否定的な感情状態(例:不快気分、不安、易刺激性)を特徴とする、再発性のCNS障害です。神経適応は解毒後も持続し、個人が薬物を利用できるようになった際の渇望と再発の原因となります。過去40年間の研究により、SUDの根底にある神経生物学の理解が大幅に進展し、治療の改善につながっています。実験動物と人間におけるますます洗練された実験方法の使用を通じて、中毒プロセスの各段階の根底にある神経経路に関する分子レベルから行動レベルまでの詳細な情報が存在します。動物モデルは人間の精神疾患を完全に再現することはできませんが、実験動物での研究はSUDの特定の要素の調査を可能にします。神経科学と精神医学の進化に伴い、これらの要素はより具体的で扱いやすいものになっています。
表1.31-1.
物質使用障害の一般的な診断基準、DSM-5
- 意図したよりも多量に、または長期間にわたって薬物を摂取する。
- 薬物の使用を減らしたいという持続的な欲求、またはその努力が成功しない。
- 薬物を入手し、使用し、または薬物から回復するために必要な活動に多大な時間を費やす。
- 渇望、すなわち薬物を使用したいという強い欲求または衝動。
- 薬物の反復使用により、職場、家庭、または学校での主要な義務を果たすことができない。
- 薬物の使用によって引き起こされた、または悪化した、持続的または反復的な社会的または対人関係の問題があるにもかかわらず、薬物の使用を継続する。
- 薬物の使用のために、重要な社会的、職業的、または娯楽的活動を諦める、または減らす。
- 身体的に危険な状況での薬物の反復使用。
- 薬物によって引き起こされた、または悪化した可能性が高い、持続的または反復的な身体的または心理的問題があることを認識しているにもかかわらず、薬物の使用を継続する。
- 耐性:中毒効果または望ましい効果を得るために薬物の増量が必要になるか、または同量の薬物を継続して使用しても効果が著しく減弱するかのいずれか。
- 離脱:薬物離脱症候群を経験するか、または離脱症候群を緩和または回避するために薬物を摂取するかのいずれか。
DSM-5に記載されているように、SUDは、有害な結果にもかかわらず、個人が病的なパターンで薬物を誤用し続けることを示唆する、認知的、行動的、生理学的症状の集合体から構成されます。SUDの診断基準(表1.31-1参照)は、おおよそ以下の4つのカテゴリーに分類できます。
- 制御障害(基準1~4)
- 社会的障害(基準5~7)
- 危険な使用(基準8および9)
- 薬理学的(基準10および11)
中毒プロセスの段階
薬物使用、誤用、および物質使用障害(SUD)の区別を理解することは極めて重要です。薬物使用には、カフェイン、ニコチン、アルコールなどの合法的な物質の使用、およびベンゾジアゼピン、マリファナ、オピオイド鎮痛剤などの医学的に処方された薬物の使用が含まれます。薬物誤用には、違法薬物の使用、または向精神薬を非医療目的で使用することが含まれます。米国成人の約15%~16%が、人生のある時点で薬物誤用に関与すると推定されています。そのうち、約3%がSUDを発症します。これには、SUDの発現には薬物使用(薬物曝露)が必要であり、薬物摂取量が増えるにつれて有害な結果にもかかわらず強迫的な薬物使用につながるという考えが暗黙的に含まれています。
偶発的な薬物使用からSUDへの移行は、衝動的使用から強迫的使用への変化、および正の強化メカニズムから負の強化メカニズムへの移行によって引き起こされる快楽調節不全として、神経生物学的に概念化されてきました。強化とは、反応と同時に刺激が与えられたり取り除かれたりすることによって、その後の反応の確率を高める動機付けプロセスです。これには2つの形態があります。多幸感に関連する正の強化(例:薬物の初期の「ハイ」)、および嫌悪状態の停止に関連する負の強化(例:薬物離脱)です。SUDを発症する偶発的な薬物使用者は、衝動制御障害の特性を示します。衝動的な行為の前に緊張感や興奮が増し、行為が行われた後に安心感や快感が生じます。衝動制御障害には正の強化メカニズムが関与していると考えられています。対照的に、SUDの基準を満たす個人は、強迫障害の特性を示します。強迫的で反復的な行動に従事する前に不安やストレスの感情があり、強迫的な行動が行われた後にストレスからの解放が生じます。強迫障害には負の強化メカニズムと習慣的で自動的な行動が関与していると考えられています。この精神医学的・動機付けフレームワーク内で見ると、SUDの発症は、乱用・中毒、離脱・負の感情、および没頭・予期という3段階のサイクルとして記述できます(図1.31-1)。衝動性は初期段階で最も顕著であり、強迫性は後期段階で優勢になります。物質使用からSUDへの移行には、感情状態、運動パターン、および認知を調節する神経回路内の各段階での病理的神経可塑性が関与しています。
乱用・中毒
最初の薬物使用は、脆弱な個人で始まることがあります。しかし、脆弱性を構成するものや薬物使用を開始する理由は個人間および文化間で異なるため、薬物使用のこの初期段階を研究することは困難です。さらに、偶発的に薬物を使用する人のごく一部(20%)しかSUDを発症しないことは、SUDへの感受性の増加が普遍的ではないことを示しています。実際、DSM-5は、SUDとは別に薬物中毒の診断基準を提供しています。個人が薬物を試すかどうか、および初期の中毒の快楽的価値は、遺伝的要因、生得的特性(例:決断力および運動衝動性、感覚探索、負の緊急性、リスクテイク)、社会的および環境的影響(例:社会経済的地位、教育、ストレス、トラウマや虐待などの逆境への曝露、同調圧力、薬物の入手可能性)、および精神医学的併存疾患(例:うつ病、不安症)の複合的な影響を受けます。これらの複雑さにもかかわらず、最近の研究は、SUDへの素因を予測する可能性のあるいくつかの重要な行動的および生物学的マーカーの特定を開始しています。薬物摂取の獲得に寄与すると考えられる生得的または環境的要因を反映する動物モデルが開発されています。これらのモデルは、SUDサイクルの乱用・中毒段階を反映する行動パラダイムで引き続きテストされています(表1.31-2)。
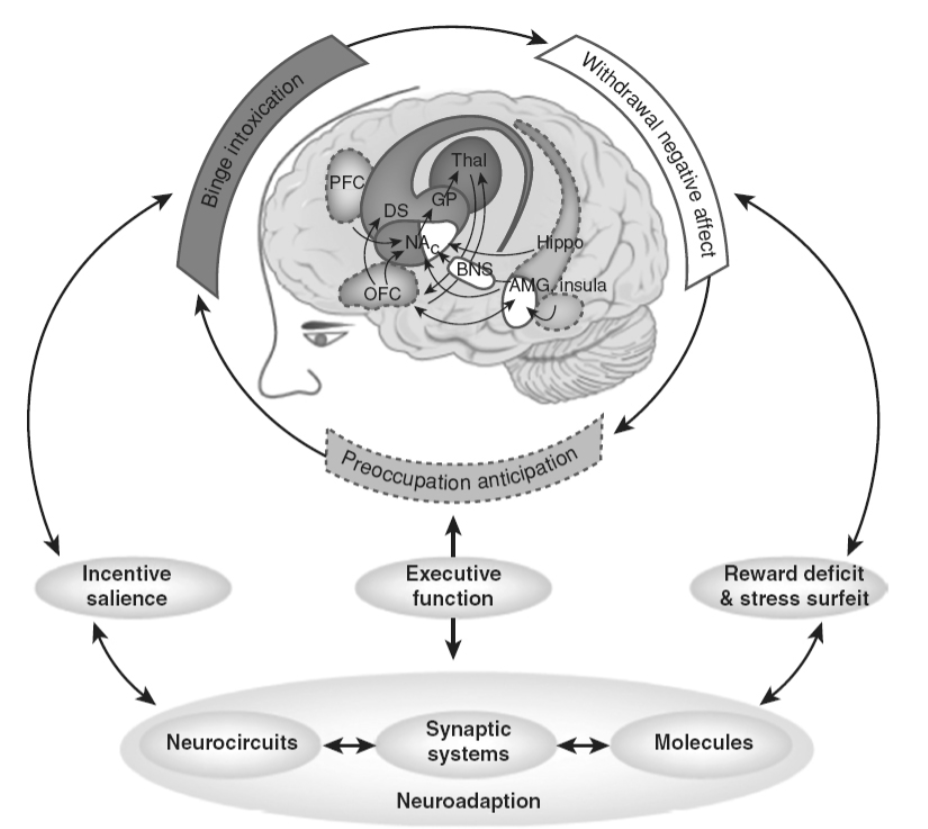
図1.31-1. 依存サイクルを3つの段階に分けた神経回路図:乱用・中毒(濃い灰色)、離脱・負の感情(白)、没頭・予期(薄い灰色)。
関与する神経回路も色分けされており、乱用・中毒段階の主要な要素として、側坐核(NAc)、背側線条体(DS)、淡蒼球(GP)、視床(Thal)を含む大脳基底核が示されています。離脱・負の感情段階の主要な要素として、扁桃体中心核(AMG)、分界条床核(BNST)、側坐核(NAc)の殻領域における移行領域を含む広範な扁桃体が示されています。そして、没頭・予期段階の主要な要素として、前頭前野(PFC)、眼窩前頭皮質(OFC)、海馬(Hippo)、島(Insula)を含む前頭皮質とアロ皮質が示されています。分子レベル、シナプスレベル、および神経回路レベルでの神経適応が組み合わさることで、依存への移行における4つの主要な要素、すなわち誘因顕著性の増加、報酬の減少、ストレスの増加、および実行機能の低下が生じます。(Wise RA, Koob GF. The development and maintenance of drug addiction. Neuropsychopharmacology. 2014;39:254-262, Springer Nature. doi:10.1038/npp.2013.261より転載。)
離脱・負の感情
物質使用がSUDへと進行するにつれて、慢性的な薬物使用期間の後には、通常、禁断期間と、ますます重症化する身体的および/または心理的離脱症状が続きます。SUDを持つ人々は、離脱状態を「飢え」またはさらなる薬物摂取によってのみ満たされる主要な欲求(すなわち、負の強化)として表現しています。薬物使用がエスカレートし、その性質が強迫的になるにつれて、神経適応が発達し、実行機能障害(例:抑制制御の低下)と、自然な報酬への動機を上回る薬物への動機付けの増加を引き起こします。動機とは、行動を活性化する生物学的、感情的、社会的、および認知的力を指し、物質使用からSUDへの移行に伴う、薬物によって誘発される快楽的および感情的状態の変化によって調節されます。これは、動機の拮抗プロセス理論(図1.31-2)において概念化されています。ソロモンとコービット(1974)によれば、「快楽的、感情的、または情動的な状態は、快楽感情(快いものも嫌悪的なものも)の強度を低下させる中枢神経系メカニズムによって自動的に拮抗される」とされています。薬物使用に対する正の快楽反応(すなわち、多幸感、報酬)は、薬物摂取後すぐに発生し、薬物の強度、質、持続時間と密接に関連し、耐性を示します。薬物離脱時には、負の感情状態が露呈します。これらは発達が遅く、消失も遅く、薬物への反復曝露によってその大きさを増します。SUDの文脈では、拮抗プロセスは薬物摂取の初期段階から始まり、報酬とストレス応答を制御する神経回路における代償的変化を反映しています。
動物モデルを用いた物質使用障害の段階研究
Table 1.31-2.
| 段階 | 強化源 | 動物モデル |
| 乱用・中毒 | ポジティブ強化 | 条件付け場所選好、薬物自己投与、選択手続き、脳刺激報酬の増加 |
| 離脱・負の感情 | ネガティブ強化 | 不安様反応の増加、脳刺激報酬の減少、条件付け場所嫌悪、依存時の薬物自己投与への動機付けの増加 |
| 没頭・予期 | 条件付けられたポジティブ強化 / 条件付けられたネガティブ強化 | 薬物、手がかり、ストレス誘発性の薬物探索再燃、長期禁断症状 |
Koob G, Kenneth Lloyd G, Mason B. Development of pharmacotherapies for drug addiction: a Rosetta Stone approach. Nat Rev Drug Discov. 2009;8:500-515, Springer Nature. doi: 10.1038/nrd2828 より改変。
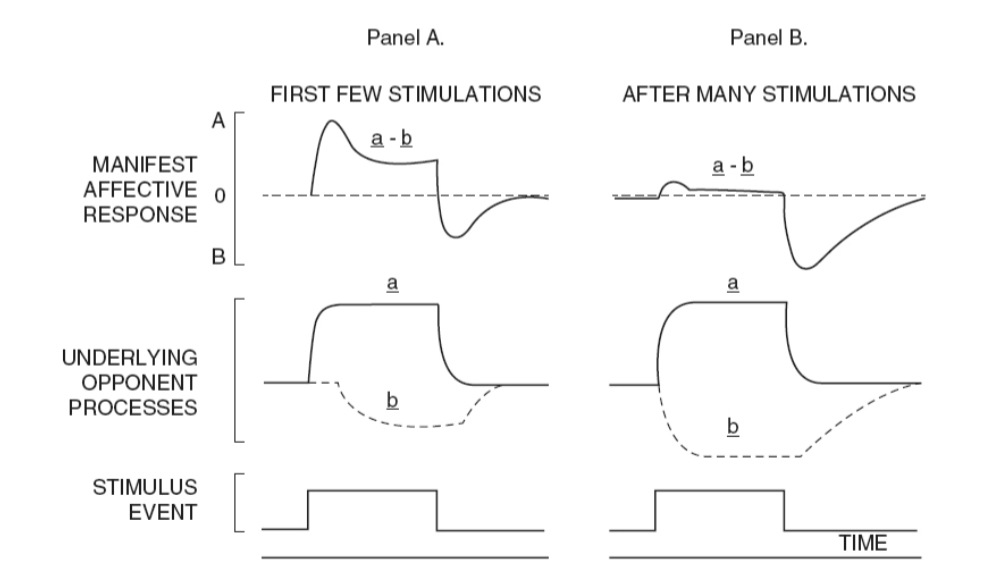
図1.31-2. 拮抗プロセス理論。パネルA:最初の数回の刺激に対する加算装置の動作。パネルB:繰り返し刺激を与えられた後の加算装置の動作。
基礎となる拮抗プロセス(中央の模式図)「a」と「b」の合計が、明示的な感情反応(上段の模式図)を生み出します。薬物乱用の文脈では、明示的な感情反応「A」は急性薬物報酬を表し、「B」は刺激停止時に現れる薬物反対効果(嫌悪)を表します(下段の模式図)。(Copyright C 1974, American Psychological Association. Solomon RL, Corbit JD. An op-ponent-process theory of motivation: I. Temporal dynamics of affect. Psychol Rev. 1974;81(2):119-145. doi:10.1037/h0036128 より許可を得て複製。)
没頭・予期
薬物離脱の期間に続いて、渇望と再発が生じます。この際、ストレス、薬物自体への曝露、以前に薬物と対になった環境手がかりといった様々な誘因が、薬物探索行動と薬物摂取行動を再燃させます。主観的な渇望の経験はしばしば再発に先行します。渇望は、薬物使用を「欲しがり/予期する」ことによって特徴づけられる、後天的な欲求と定義できます。その重要性は、DSM-5のSUD診断基準に組み込まれていること(表1.31-1参照)によって例示されます。向精神薬使用障害を持つ人々の研究では、渇望レベルの増加は、不安、易刺激性、落ち着きのなさ、心拍数の増加、吐き気など、ストレス関連の興奮と重なり合う症状の増加と関連しており、これらは薬物使用によって一時的に軽減されます。
実験室での渇望の客観的測定は、これまで研究者にとって大きな課題でした。しかし、動物モデルは、薬物摂取および薬物探索行動の様々な客観的かつ定量化可能な指標を提供し、そこから渇望の神経生物学的基盤を推測できます。薬物探索および薬物摂取行動のメカニズムを研究する上で最適な経験的モデルは、自己投与(静脈内[IV]、蒸気、または経口経路)であり、薬物の強化効果を測定するための確立されたオペラント手続きです。動物における薬物自己投与は、表面妥当性、構成概念妥当性、および予測妥当性の基準を満たしています。動物は人間と同様に、偶発的に薬物を自己投与します。IVおよび吸入経路は、薬物を脳に迅速に送達できるため、非常に強化効果が高いです。動物における薬物自己投与研究は、SUD治療のための推定される薬物療法の前臨床評価にも広く使用されています。前臨床研究は、動物における薬物の強化効果を媒介する根底にあるメカニズムと神経回路が、人間における薬物関連効果を媒介するものと実質的に重なることを示唆しています。これらの研究はまた、報酬関連行動の神経基盤の正常な機能の理解を深めました。
臨床介入は、離脱症状を最小限に抑えながらSUD患者を薬物から遠ざけること(解毒)に成功しています。しかし、これらの患者の禁断状態を維持するための臨床介入は、その効果が限られています。したがって、再発の神経生物学的基盤の研究は特に重点が置かれてきました。なぜなら、SUDのサイクルにおけるこの点は、この障害の慢性化の根底にあり、再発の防止は成功する治療アプローチにとって極めて重要だからです。薬物自己投与パラダイムは、以前に薬物送達と関連付けられていたオペラント行動(すなわち、レバー押しや鼻突き)の再燃に焦点を当てることで、再発をモデル化するために適用されてきました。「再燃」は、「薬物探索行動の再燃」の一般的な略語であり、薬物渇望と再発の動物モデルです。この手続きでは、実験動物は乱用薬物を自己投与するように訓練され、その後、オペラント反応が薬物送達と対にならなくなる消去訓練、または禁断のいずれかの期間に置かれます。消去条件下でのオペラント反応の所定の基準が達成されると、薬物プライム、個別手がかり、文脈手がかり、またはストレス因子の提示によって、動物の薬物探索行動の再燃がテストされます。動物における再燃モデルは、人間における再発をより密接に近似するようにさらに改良できますが、薬物依存の人間における様々な刺激によって引き起こされる薬物渇望と再発の活性化をモデル化するための優れた表面妥当性と構成概念妥当性を持っています。
依存症の理論
物質使用障害(SUD)の発症と維持を説明するために、いくつかの理論が提唱されてきました。この疾患の異質性(例:遺伝子、環境、薬物自体の寄与)を考慮すると、それぞれの理論の側面が特定の条件下で適用可能である可能性が高いです。主要な理論を以下にまとめ、上記のSUDサイクルおよび図1.31-1の文脈で整理します。これらの理論が相互に排他的ではなく、むしろSUDサイクルの特定の側面を強調する傾向があることに注意することが重要です。ポジティブ強化がサイクルを開始し、最終的に習慣的かつ強迫的になる初期の薬物摂取の反復につながるという点で、一般的な合意があります。
精神運動刺激理論
依存性薬物には共通の特徴があります。それらは精神運動活性化を引き起こし、強化作用を持ち、接近行動を誘発します。1960年代から1980年代に行われた画期的な研究により、中脳皮質辺縁系ドーパミンシステムが自然な接近システムの主要な神経基盤であることが示されました。この理論では、薬物誘発性のドーパミン放出が強化効果を持ち、反復的な薬物「接近」をもたらす運動システムを活性化するため、人々は薬物摂取行動を開始し、維持するとされています。
誘因感作理論
この理論は、依存症の精神運動刺激理論を基盤としており、薬物が、通常は動物が種の保存に重要な顕著な刺激(例:獲物の匂い)に接近するよう動機付ける神経システム(例:中脳皮質辺縁系ドーパミンシステム)を乗っ取ると仮定しています。文脈、手がかり、その他の刺激(乱用薬物を含む)がこれらの神経システムを活性化すると、誘因顕著性(動機付けの重要性、「欲求」)が付与されます。この理論は、乱用薬物への反復曝露がこれらのシステムに持続的な神経適応をもたらし、動物が薬物や薬物と関連付けられた手がかりに対して過敏になることを提唱しています。したがって、SUDが発症するにつれて、その人の動機付けの焦点は、自然な報酬探索を犠牲にして薬物探索に狭まります。この理論の重要な側面は、誘因顕著性(薬物「欲求」)を制御する神経システムの感作が、報酬(薬物「好き」)を制御する神経システムの変化とは独立していることです。最後に、この理論の提唱者は、誘因顕著性を媒介するシステムが、薬物離脱によって誘発される負の快楽状態を制御するシステムとは異なると主張しています。
逸脱学習理論
自然な報酬を犠牲にして薬物や薬物手がかりの誘因顕著性が増加することは、逸脱学習の文脈で説明されます。誘因感作理論と同様に、この理論は、薬物への反復曝露が、非薬物関連手がかりに対する正常な反応を制御する神経システムを調節することにより、薬物関連手がかりへの反応性を高めると考えます。この逸脱学習プロセスは、関連付けられた脳構造の変化を表し、薬物探索と摂取が自動的または習慣的になるものと考えられています。このプロセスが腹側線条体から背側線条体への段階的な移行によって媒介されるという考えを支持する証拠があります。この理論の重要な側面は、薬物および薬物手がかりに対する感作された反応性が罰に影響されないことであり、その結果、SUDの中心的症状である「有害な結果にもかかわらず薬物使用を継続する」が生じます。
前頭線条体機能不全理論
この理論は、SUDを持つ人々が衝動制御が不十分であるという臨床的観察を説明するためのメカニズムを組み込んでいます。反復的な薬物曝露が皮質および辺縁系の回路に変化をもたらし、個人が薬物および薬物手がかりに対して病理的な反応を示す一方で、薬物摂取行動に対する抑制的な「トップダウン」の実行制御が同時に障害されると提案しています。これにより、衝動制御の喪失、劣悪な意思決定、薬物関連手がかりへの反応性の亢進、そして強迫的な薬物使用につながります。
快楽アロスタシス理論
この理論は、動機の拮抗プロセス理論に根ざしており、初期の薬物誤用は薬物の報酬効果から得られるポジティブ強化によって動機付けられるのに対し、慢性の薬物誤用は、ストレス関連システムの動員と「ハイパーカティフェイア(hyperkatifeia)」と呼ばれる極端に負の快楽的および感情的状態の出現に起因するネガティブ強化によって動機付けられると仮定しています。この慢性的な薬物誘発性アロスタシス的快楽状態は、動物の正常な報酬設定点における持続的な変化を反映しています。快楽アロスタシスは、皮質、線条体、視床領域を結びつける回路を介するネガティブ強化メカニズムを通じて、強迫的な薬物摂取に寄与します。
依存症における脳の経路
動物モデルと人間の研究から、すべての乱用薬物が脳の辺縁系にある共通の回路に収束するというかなりの証拠があります。数十年にわたる研究を総合し(そして単純化すると)、すべての乱用薬物への慢性的な曝露が作用する3つの主要な回路があります。第一に、依存性薬物への慢性的な曝露は、ドーパミンシステムの恒常性障害を引き起こし、自然な報酬(例:食べ物、水、性行為、社会的交友関係)が典型的な方法でドーパミン放出を増加させる効果が低下します。これらの恒常性変化は、薬物摂取期間の間、または薬物離脱および禁断期間中に観察される負の感情状態に寄与すると考えられています。また、慢性的、間欠的な薬物曝露がドーパミンシステムを感作させ、薬物または薬物関連刺激への曝露がドーパミン作動性伝達のより大きな増加を引き起こすことも観察されています。このドーパミン応答の感作は、薬物摂取が停止した後も長く持続し、薬物渇望と再発に関連する可能性があります。すべての乱用薬物に共通する第二の神経回路は、コルチコトロピン放出因子(CRF)の視床下部外作用を含みます。急性薬物離脱は、扁桃体内のCRF含有ニューロンを活性化し、これらは後述する多数の前脳および脳幹領域に投射します。CRFのストレス様効果は、薬物離脱時に発生する負の感情的および身体的症状に寄与すると考えられています。ほとんどの薬物クラスへの慢性曝露に共通するもう一つの適応は、様々な脳ネットワーク(例:顕著性、報酬、実行機能、記憶、習慣)の活動低下です。特に関連性が高いのは、皮質の「低前頭機能」であり、皮質ニューロンの基礎活動が低下し、自然な報酬が前頭前野、ACC、眼窩前頭皮質などの特定の皮質領域を活性化する能力が低下します。これらの皮質領域は、側坐核および腹側被蓋野(VTA)へのグルタミン作動性投射を介して、実行機能、作業記憶、注意、および行動抑制を制御します。これらの前頭皮質領域およびそのグルタミン作動性出力における慢性的な薬物誘発性神経適応は、SUDの衝動的および強迫的側面の両方に寄与すると考えられています。
急性薬物報酬の根底にある神経経路
DSM-5は、物質中毒、離脱、SUDを異なる診断カテゴリーに分けています。中毒は4つの基準(表1.31-3)から構成され、そのうち2つは物質摂取中または摂取後すぐに生じる多幸感を含みます。多幸感以外の効果も確かに強化作用を持つことがありますが、このセクションでは、乱用薬物の急性報酬効果において役割を果たすことが知られている脳の経路に焦点を当てます。この中毒の特徴が、薬物摂取を強化し、脆弱な個人でSUDにつながると考えられています。
表1.31-3.
物質中毒の一般的な診断基準、DSM-5
A. 物質の最近の摂取。
B. 物質摂取中またはその直後に生じる、臨床的に重要な問題のある行動的または心理的変化。
C. 物質特有の生理学的/心理的症状の最小数。
D. 徴候または症状は、別の医学的状態に起因するものではなく、別の精神障害(他の物質による中毒を含む)によってよりよく説明されるものではない。
ªDSM-5には、大麻、吸入剤、オピオイド、および覚せい剤の多幸感が含まれます。
1950年代に、ラットが特定の脳領域に電気刺激を自己投与するためにレバーを押すことを学習する(頭蓋内自己刺激 [ICSS] として知られるオペラント行動)という発見は、報酬機能に関与する神経回路の発見を可能にしました。脳刺激報酬を生み出すICSSの有効性は、オペラント反応を支持する電気刺激の最小周波数などの尺度によって定量化されます。脳刺激報酬には複数の脳領域が関与しますが、最も感受性の高い部位(最も低い刺激閾値によって定義される)は、外側視床下部レベルの内側前脳束内にあります。内側前脳束は腹側被蓋野(VTA)を前脳基底部に接続し、上行性のノルエピネフリンおよびドーパミンのモノアミン作動性線維を運びます(図1.31-3)。ほとんどの乱用薬物の急性投与は、脳刺激報酬閾値を低下させ(すなわち、報酬を増加させ)、慢性投与は離脱中に報酬閾値を増加させます(すなわち、報酬を減少させます)。要約すると、これらの初期の研究は、モノアミン作動性神経伝達が乱用薬物の強化効果の重要な基盤であるという強力な支持を提供しました。
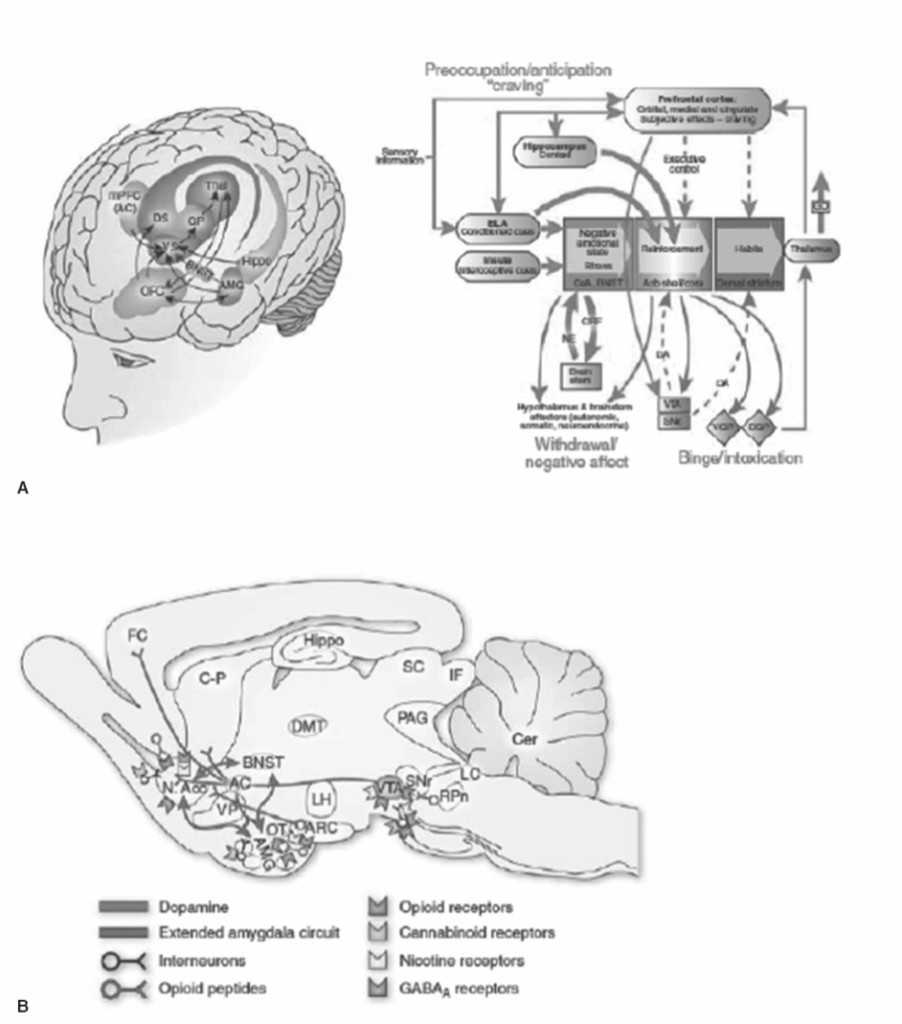
図1.31-3. 物質乱用および物質使用障害に関与する神経回路図。A:依存サイクルの3つの段階に必要な脳回路内で生じると考えられる神経適応の組み合わせを示す模式図。
前頭皮質システムが障害され、実行機能に欠陥が生じ、自然な強化因子と比較して薬物の誘因顕著性に寄与します。ドーパミンシステムが障害され、CRFなどの脳ストレスシステムが活性化され、嫌悪的な不快状態の文脈で薬物および薬物関連刺激の顕著性をさらに再設定します。(Aの左図は、Koob GF, Everitt BJ, Robbins TW. Reward, motivation, and addiction. In: Squire LG, Berg D, Bloom FE, Du Lac S, Ghosh A, Spitzer N, eds. Fundamental Neuroscience. 3rd ed. Academic Press; 2008:987-1016より転載。)B:代表的なげっ歯類の脳の矢状断面図で、乱用薬物の急性強化作用に関与する経路と受容体システムを示しています。
青い矢印は、薬物強化において重要な機能を持つと仮定される広範な扁桃体システム内の相互作用を表しています。AC, 前交連; AMG, 扁桃体; ARC, 弓状核; BNST, 分界条床核; Cer, 小脳; CP, 尾状核-被殻; DMT, 背内側視床; FC, 前頭皮質; Hippo, 海馬; IF, 下丘; LC, 青斑核; LH, 外側視床下部; N Acc., 側坐核; OT, 嗅覚路; PAG, 中脳水道周囲灰白質; RPn, 網様橋核; SC, 上丘; SNr, 黒質網様部; VP, 腹側淡蒼球; VTA, 腹側被蓋野。(カラー画像はeBook参照。)(Bは、Koob GF. The neurocircuitry of addiction: implications for treatment. Clin Neurosci Res. 2005;5(2-4):89-101. Copyright @ 2005 Association for Research in Nervous and Mental Disease. doi: 10.1016/j.cnr.2005.08.005より転載。)
中脳辺縁系ドーパミン経路の活動が精神刺激薬の主要な強化効果に必要であるものの、他の薬物クラスではより「促進的」な機能を持つという新たなデータが蓄積されています。これらの違いは、各薬物クラスの多様な薬理学的作用機序によるものです。コカインやアンフェタミンなどの精神刺激薬は、神経終末でモノアミン再取り込み輸送体を遮断し、ドーパミンや他のモノアミンのレベルを直接増加させますが、他の薬物は中脳皮質辺縁系経路を間接的に活性化させます(図1.31-4)。オキシコドンやヘロインなどのオピオイドは、VTAのμ-オピオイド受容体に作用して抑制性GABA介在ニューロンの活動を低下させ、その結果、前脳領域でのドーパミン放出がより多くなります。ニコチンやカンナビノイドを含む他の薬物は、それぞれの受容体を活性化し、ドーパミンニューロンの脱抑制または興奮を引き起こします。アルコールを含む、より複雑な薬理学的プロファイルを持つ薬物も、セロトニン作動性、グルタミン酸作動性、GABA作動性受容体など、さまざまな受容体サブタイプへの作用を介してではありますが、ドーパミン放出の増加につながります。やや議論の余地はありますが、これらの物質の一部(例:オピオイド、フェンサイクリジン、アルコール、ベンゾジアゼピン)の報酬効果は、ドーパミンとは独立して、側坐核の中型有棘ニューロンに直接作用することによって調節される可能性があるという理論もあります。
中脳皮質辺縁系ドーパミン経路は、すべての乱用薬物の共通の神経基盤として一貫して特定されています。実際、げっ歯類の研究では、依存性のある可能性のあるすべての薬物が、側坐核などの前脳構造におけるドーパミン放出を増加させることが示されています(図1.31-3参照)。ドーパミン細胞の大部分は腹側中脳、特にVTAに存在し、側坐核、前頭前野、扁桃体などの前脳領域に投射しています。急性薬物報酬におけるこの経路の重要性の例として、VTAまたは側坐核の病変がげっ歯類における薬物の自己投与を妨げることが示されています。また、コカイン、ヘロイン、またはアルコールのような薬物はVTAに直接自己投与される一方で、VTAのドーパミンニューロンの抑制は薬物自己投与を抑制します。一般に、非薬物報酬(例:食物)への反復曝露は、中脳皮質辺縁系ドーパミン経路を異常な(多すぎたり少なすぎたりする)ドーパミン放出を引き起こさない一貫した方法で活性化させます。対照的に、乱用薬物は、急性薬物摂取がドーパミン放出の劇的かつ超正常な増加を引き起こし、その後の薬物への反復曝露と介入離脱期間の後に、深く長期にわたる適応変化が生じるように、この経路を「乗っ取ります」。過去数十年にわたる研究は、ドーパミンの複数の役割を特定してきました。それは環境中の刺激に顕著性を付与し、行動の活性化と目標指向性行動の実行を促進します。ドーパミンシグナル伝達の時間経過も重要な要素です。急速な位相性ドーパミンニューロン発火は、報酬体験と価値を符号化し、予測刺激と報酬および罰との関連付けを学習するために必要です。一方、ドーパミンニューロンの持続性発火は、学習された手がかりに反応する際の全体的な動機付け状態を決定します。
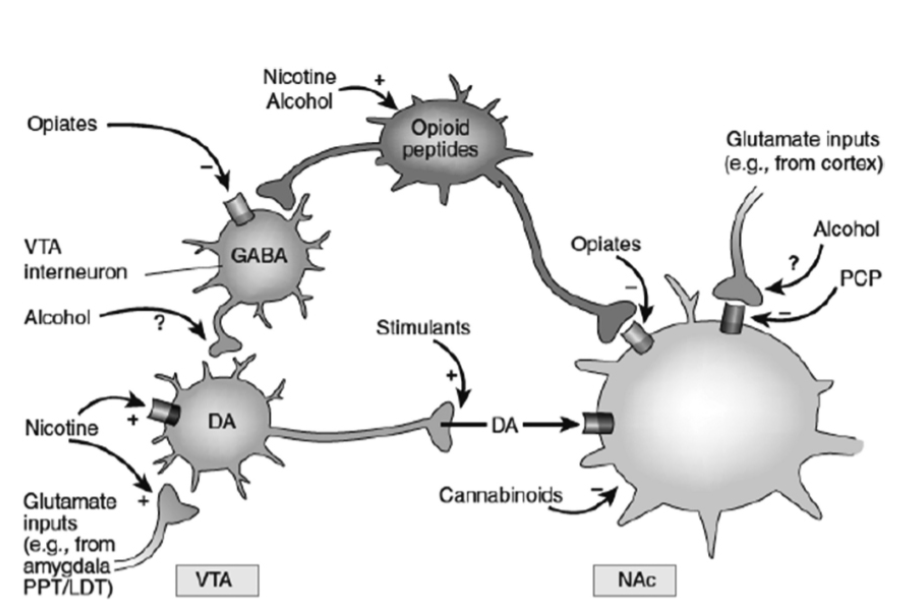
図1.31-4. 乱用薬物のVTA-NAc経路に対する収束的な急性作用の簡略模式図。
覚せい剤は、**側坐核(NAc)**におけるドーパミン作動性伝達を直接増加させます。アヘン剤は、**腹側被蓋野(VTA)**のGABA作動性介在ニューロンを抑制することにより、NAcにおけるドーパミン作動性伝達を間接的に増加させ、これによりVTAドーパミン(DA)ニューロンを脱抑制します。アヘン剤はまた、NAcニューロン上のμ-オピオイド受容体にも直接作用します。μ-オピオイド受容体は、D2ドーパミン受容体と同様に、抑制性Gタンパク質Gαiを介してシグナル伝達を行うため、これら2つのメカニズムは一部のNAcニューロン内で収束します。他の乱用薬物の作用はより推測の域を出ません。ニコチンは、VTAドーパミンニューロン上のニコチン性コリン作動性受容体を刺激することでVTAドーパミンニューロンを直接活性化し、ドーパミン細胞を支配するグルタミン酸作動性神経終末上の受容体を刺激することで間接的に活性化するように見えます。アルコールはGABAA受容体機能を促進し、これによりVTAのGABA作動性終末を抑制し、VTAドーパミンニューロンを脱抑制する可能性があります。同様に、NAcニューロンを支配するグルタミン酸作動性終末も抑制する可能性があります。アルコールには、その他にも多くのメカニズムが提案されています(図には示されていません)。カンナビノイドのメカニズムは複雑であり、NAcのグルタミン酸作動性およびGABA作動性神経終末、およびNAcニューロン自体に存在するCB1受容体(D2およびμ-オピオイド受容体と同様にGαi結合型)の活性化を伴います。**フェンサイクリジン(PCP)**は、NAcのシナプス後NMDAグルタミン酸受容体を抑制することで作用する可能性があります。最後に、ニコチンとアルコールが内因性オピオイド経路を活性化する可能性があり、これらおよび他の乱用薬物(アヘン剤など)が内因性カンナビノイド経路を活性化する可能性があるといういくつかの証拠があります(図には示されていません)。PPT/LDT, 脚橋被蓋核/外側背側被蓋核。(Nestler E. Is there a common molecular pathway for addiction? Nat Neurosci. 2005;8:1445-1449, Springer Nature. doi: 10.1038/nn1578より転載。)
側坐核は腹側線条体の小さなサブコンポーネントであり、ドーパミン依存性およびドーパミン非依存性の薬物強化の両方の基質となります。側坐核は、扁桃体、前頭皮質、海馬に由来するグルタミン酸作動性求心性神経から快楽状態に関する情報を受け取り、錐体外路運動システムとの結合を介してそれを動機付け行動に変換します。グルタミン酸神経伝達は厳密に調節されています。多すぎても少なすぎても有害な影響(例:細胞毒性)を及ぼす可能性がありますが、刺激依存的なグルタミン酸作動性伝達の変化は学習と行動への関与に必要です。実際、長年の概念として、側坐核は「動機から運動へのインターフェース」であるとされています。側坐核自体は、コアとシェル領域に細分することができ、その機能的結合と神経細胞の表現型は、動機から運動へのこの機能的統合を反映しています。シェルは、急性薬物報酬、動機付け行動、行動感作、および感情状態の変化において重要な役割を果たします。コアは腹側線条体の中央部分であり、隣接する運動関連の背側線条体の機能的連続体です。
耐性と離脱の根底にある神経経路
薬物が時間をかけて繰り返し使用されると、耐性が発現することがあります。耐性とは、薬物効果(例:多幸感)に対する感受性が低下し、初期に達成されたのと同じレベルの反応を得るためには、より高用量の薬物が必要となることと定義されます。重要なことに、耐性の発現は依存症と同義ではありません。依存症の文脈では、耐性は報酬に拮抗するメカニズムを関与させ、逆説的に薬物探索行動を強化します。拮抗プロセス理論は、耐性と偶発的な薬物使用から依存症への移行を理解するための枠組みとして使用されてきました。薬物の即座の報酬効果に続いて、薬物依存的な拮抗プロセスの動員による遅延性の嫌悪効果が生じます(図1.31-2参照)。これらの嫌悪効果は薬物離脱中に強く現れ、MDD(大うつ病性障害)に似た不安、無快感症、易刺激性、抑うつ気分を含む急性および遷延性の嫌悪状態を含みます。薬物に対する耐性と拮抗プロセスの根底にあるメカニズムは、分子レベル、細胞レベル、および回路レベルで発生し、「システム内」または「システム間」適応として分類できます。
慢性的な薬物投与に対する「システム内」神経適応の主要な例は、離脱時の中脳皮質辺縁系ドーパミン系の機能低下であり、これにより非薬物関連刺激への動機付けが低下し、誤用薬物への感受性および動機付けが増加します(図1.31-3A参照)。中脳皮質辺縁系ドーパミン系の機能低下と一致して、人間における精神刺激薬の離脱は、疲労、抑うつ気分、倦怠感と関連しており、動物では自然な報酬を得るための労働意欲の低下および運動活動の低下と関連しています。同様に、慢性的なオピオイドからの離脱は、脳が薬物の存在下で平衡を保とうとした試みで生じたすべての神経適応を本質的に露呈させます。結果として、消化管機能から感情状態まで、すべてを調節する神経回路は瞬時に不均衡になり、オピオイド離脱症候群が現れます。不安、不快気分、抑うつ、易刺激性などの感情的な離脱症状の原因の一つは、ドーパミンニューロンの発火および側坐核などの遠心性標的におけるドーパミン放出の減少であると考えられています。
脳の「報酬センター」としての長い歴史にもかかわらず、側坐核と腹側淡蒼球が、正および負の環境刺激を接近または回避行動のいずれかに処理する二価性構造であるという考えを支持する証拠が増加しています。過去数年間に収集された電気生理学的データは、側坐核が固有の中型有棘ニューロンの発火率の増加を介して嫌悪状態を符号化する可能性があり、個々の側坐核ニューロンが刺激に対する発火率応答を変化させることによって刺激の快楽価を追跡できることを示しています。腹側淡蒼球では、食欲刺激と嫌悪刺激はそれぞれ異なるニューロン集団、すなわちGABAニューロンとグルタミン酸ニューロンによって符号化されます。乱用薬物が側坐核と淡蒼球に双曲的な正の(薬物の「ハイ」)および負の(薬物離脱、「クラッシュ」)感情シグナルを提供し、薬物依存症が嫌悪的な結果に対する無感受性を特徴とするため、これは依存症の理解に重要な影響を及ぼします。
システム間神経適応も耐性および離脱症候群に寄与します。これらには、ノルエピネフリン、CRF、オレキシン、ダイノルフィン、サブスタンスP、バソプレシン、神経ペプチドY(NPY)、エンドカンナビノイド、オルファニン、その他多数の乱用薬物によって直接標的とされない神経化学システムが関与します。広範な扁桃体は、扁桃体中心核、分界条床核(BNST)、および側坐核シェルの内側部分から構成され、ストレスシステムと報酬システムを統合して薬物離脱誘発性のハイパーカティフェイアを生み出し、SUDの発症に関連するネガティブ強化プロセスを促進する共通の解剖学的基盤を表しています(図1.31-3A参照)。広範な扁桃体の関与は、脳が薬物の慢性的存在にもかかわらず正常な機能を回復しようとするメカニズムの一つです。ストレスペプチドCRFは、HPA軸と広範な扁桃体の両方のストレス応答を媒介し、CRFはすべての主要な乱用薬物の離脱中に放出されます。要約すると、薬物離脱は、システム内における中脳皮質辺縁系ドーパミン活動の減少と、システム間におけるストレス様神経伝達物質システムの動員と関連しています。
乱用薬物への慢性曝露は、中脳皮質辺縁系および広範な扁桃体回路内のCRFおよびダイノルフィンシステムの活動を増加させます。一般に、CRFとダイノルフィンは、離脱とストレスの両方の特徴を持つ状態を生み出します。ダイノルフィンはκ-オピオイド受容体(KOR)に結合して活性化し、CRFは脳内のCRFタイプ1および2受容体(CRF1-R、CRF2-R)に結合して活性化します。VTAおよび側坐核を含む中脳辺縁系構造におけるKOR活性化はドーパミン伝達を減少させますが、CRFの効果はより複雑です。全体として、ストレスがCRF放出を引き起こし、それが神経ストレス回路内のダイノルフィン放出およびその後のKORシステムの活性化を増加させるという、2つのストレスペプチドシステム間の連続的なCRFからダイノルフィンへの方向性関係を支持する証拠があります。乱用薬物からの離脱は、CRFおよびダイノルフィン放出によって符号化される不快な状態を引き起こすストレス因子として概念化できます。これは、VTAへのCRF注入が薬物探索の再燃を引き起こす可能性があること(おそらくドーパミンニューロンの活性化を介して)、およびCRF拮抗薬がストレス誘発性の薬物探索再燃は減少させるが、薬物誘発性の再燃は減少させないという研究によって裏付けられています。同様に、KOR拮抗は、コカイン離脱誘発性の無快感症の発症と発現を阻害し、ラットにおけるニコチンおよびモルヒネ離脱症状の発現を減弱させます。KOR誘発性の不快気分は、乱用薬物の報酬価を高めると考えられています(ただし、経験的証拠は主に精神刺激薬に集中しています)。依存行動におけるKORのこの役割は、ストレス誘発性の薬物探索再燃における役割を含むように拡大されました。げっ歯類では、KOR拮抗およびダイノルフィン遺伝子の遺伝的欠失は、ストレス誘発性の薬物探索再燃を阻害しますが、コカインプライム誘発性の再燃は阻害しません。
物質使用障害の根底にある神経経路
制御障害(衝動的強迫的使用)
薬物への反復曝露は、前頭前野と腹側線条体のD1受容体発現中型有棘ニューロン間の経路を増強します。これは、薬物への反復曝露後の薬物探索行動の活性化の根底にあると考えられています。SUDの発症と進行のもう一つの側面は、反復的な薬物曝露に伴う、自発的(目標指向的、モデルベース)な薬物使用から習慣的(モデルフリー)で強迫的な薬物使用への移行です。最近のデータは、これが薬物探索および薬物摂取行動に対する腹側から背側線条体への薬物依存性制御の移行を介して符号化されることを示しています(図1.31-5)。これは、刺激剤、ニコチン、アルコールのSUDで実証されています。1線条体への皮質入力の基本的な組織は、辺縁系から連合野、そして運動野への機能的勾配で構成されています。同様の勾配は、中脳から側坐核への接続にも見られます。内側(すなわちシェル)から外側(すなわちコア/背側線条体)への一連の投射ループが、辺縁系関連構造からの感情に基づく情報を大脳基底核の運動関連領域に伝達することを可能にする地形的組織が存在します。側坐核(腹側線条体)がSUDの発症に寄与する報酬的な薬物効果にとって特に重要な基質であるのに対し、背側線条体はSUDを維持する運動習慣にとって特に重要な基質であると概念化されてきました。SUDが発症するにつれて、自発的な薬物使用から習慣的な薬物使用への移行というこの現象は、眼窩前頭から内側背側線条体回路の活動増加と関連していることが示されました。これは、関連する有害な結果と比較した薬物価値の過大評価を反映していると考えられています。このような発見は、アルコールまたは覚せい剤SUD患者における背側線条体でのドーパミン放出と手がかり反応性の増加を示す一方、娯楽的に薬物を使用する被験者では腹側線条体でのみドーパミン放出と手がかり反応性の増加を示す人間の機能的脳画像研究と広く一致しています。2
要約すると、前頭前野、線条体、および中脳ドーパミンニューロン間の接続は、線条体の報酬関連領域から認知および運動領域へのフィードフォワード組織を形成する上昇らせん状に組織されています。重要なことに、自発的な薬物使用から習慣的な薬物使用への移行の根底にある神経ネットワークは、薬物依存性です。例えば、ヘロイン自己投与研究では、腹側内側皮質から腹側および背側線条体回路の情報が、らせん状のフィードフォワード系列ではなく、並行して処理される可能性があることが示されています。
渇望
薬物渇望は依存症において重要な概念であり、現在ではDSM-5にSUDの臨床症状として含まれています。渇望は、その瞬間に薬物を使いたいという欲求によって特徴づけられる、後天的な欲求と定義できます。3薬物渇望は、慢性的薬物使用後、薬物および薬物手がかりの関連する顕著性の増加とともに明らかになります。臨床研究は、薬物の禁断期間または離脱期間中に生じる不安や苦痛の急性の増加は、負の強化モデルで提案されているように、それ自体で薬物の再発を予測するものではないことを示しています。むしろ、嫌悪状態と薬物渇望の同時増加が、その後の薬物摂取と再発を予測します。
渇望は、非常に個人的で主観的な感情に基づく状態であるため、SUDの動物モデルで研究することは困難です。しかし、SUD患者における渇望と薬物使用のエピソードをリアルタイムで研究する神経画像技術と生態学的瞬間評価アプローチの最近の進歩により、渇望に関与する神経回路の特定が可能になりました。非薬物文脈ではSUDにおいて異なる脳ネットワーク(例:顕著性、報酬、実行機能、記憶、習慣ネットワーク)の活動が低下しますが、薬物手がかりへの曝露はこれらの回路の神経活動を大幅に増加させ、これは手がかり反応性と呼ばれ、渇望と相関することが示されています。同様に、ストレス誘発性の渇望は異なる脳回路を活性化します。
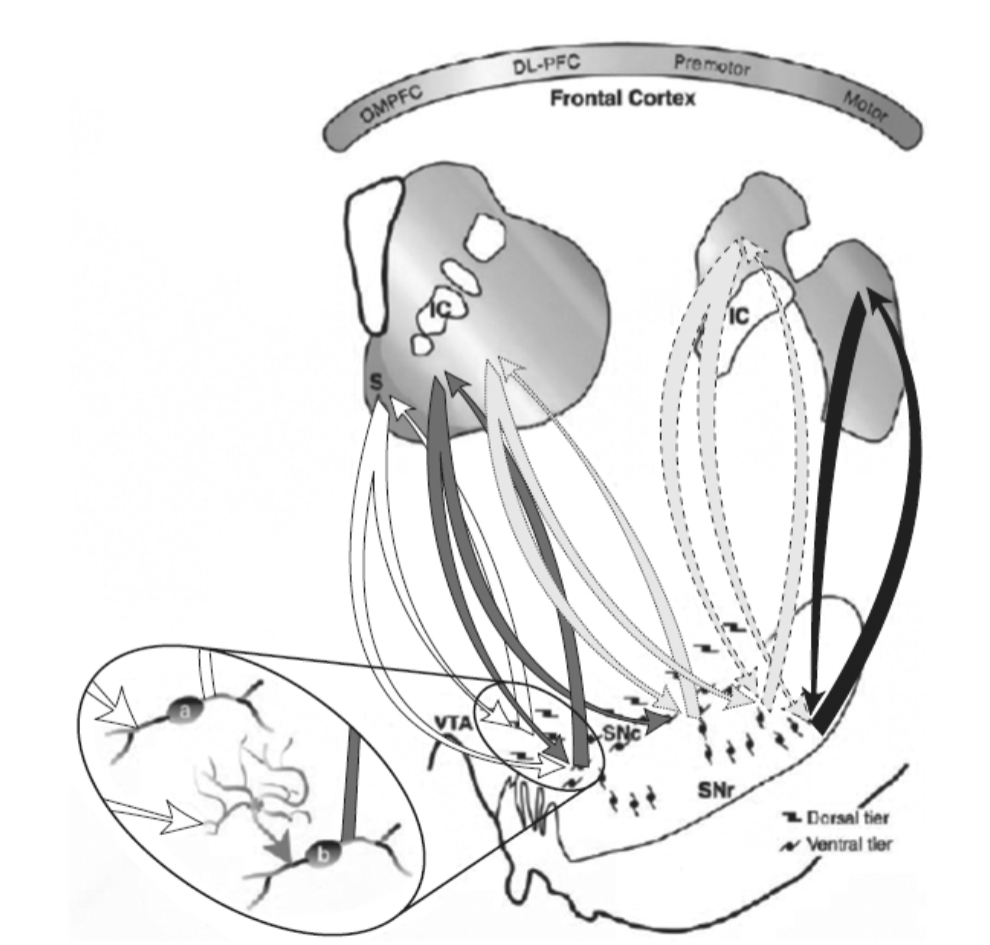
図1.31-5. 線条体黒質線条体(SNS)投射の組織図で、螺旋状の辺縁系-運動ループを構成しています。
線条体の吻側および尾側模式図の色のグラデーションは、機能的皮質線条体入力の組織を示しています(白=辺縁系、薄い灰色=連合野、黒=運動)。シェルは主に扁桃体、海馬、皮質領域25およびlaからの前脳入力を受け取ります。コアは眼窩前頭皮質全体(OMPFC)からの入力を受け取ります。背外側前頭前野(DL-PFC)は中心線条体に投射し、運動前野および運動野は背外側線条体に投射します。シェルからの中脳投射は、腹側被蓋野(VTA)と腹内側黒質緻密部(SNc)の両方を標的とします(白い矢印)。VTAから側坐核シェルへの中脳投射は、「閉じた」相互SNSループを形成します(白い矢印)。内側SNからの投射は、側坐核コアにフィードフォワードし、螺旋の最初の部分を形成します(濃い灰色の矢印)。螺旋は、コアに由来し、より背側に投射する経路(黒い矢印)を持つSNS投射(薄い灰色の矢印と点線矢印)を介して続きます。このようにして、腹側線条体領域は、螺旋状のSNS投射を介してより背側線条体領域に影響を与えます。拡大された楕円領域は、相互ループとフィードフォワードループにおけるSNS投射のシナプス相互作用の仮説モデルを示しています。各SNS投射の枝の相互成分(白い矢印)は、ドーパミン細胞に直接終末し(a)、抑制をもたらします。非相互的、またはフィードフォワード成分(濃い灰色の矢印)は、GABA作動性介在ニューロン(薄い灰色の細胞)を介してドーパミン細胞に間接的に終末し(b)、脱抑制とドーパミン細胞のバースト発火の促進をもたらします。IC, 内包; S, 側坐核シェル; SNr, 黒質網様部。(Haber SN, Fudge JH, McFarland NR. Striatonigrostriatal pathways in primates form an ascending spiral from the shell to the dorsolateral striatum. J Neurosci. 2000;20(6):2369-2382. doi: 10.1523/JNEUROSCI.20-06-02369.2000. Copyright @ 2000 Society for Neuroscienceより転載。)
再発
SUD治療における主要な問題は、禁断期間の後であっても薬物使用への再発です。実験室環境でのモデル化が困難な渇望とは異なり、再発という現象は、上記で説明した再燃手続きを用いて実験動物でうまくモデル化されています。動物研究からの証拠は、薬物のオペラント反応の消去後の薬物および手がかり誘発性の再燃に関連する神経回路の変化が、前頭前野から側坐核コアへのグルタミン酸作動性投射、VTAから内側前頭前野へのドーパミン投射、および側坐核から腹側淡蒼球へのGABA投射と関連していることを示唆しています。対照的に、ストレス誘発性の薬物探索の再燃は、広範な扁桃体内のCRFおよびノルエピネフリンシステムの活性化に依存する傾向があります。
薬物プライミングによる再発
誤用薬物の少量(しばしば「プライミング」と呼ばれる)は、人間の薬物欲求の主観的状態を開始させ、新たな薬物摂取を促す可能性があります。初期の研究では、VTAのドーパミンニューロンと、それぞれ側坐核シェルおよびコアに投射する前頭前野(前辺縁皮質、前帯状回、内側)のグルタミン酸作動性ニューロンが、コカインおよびヘロイン誘発性の薬物探索の再燃に決定的な役割を果たすことが示されました。実際、コカインおよびヘロイン探索の根底にある回路の主要な特徴は、前辺縁皮質からの求心性神経による側坐核コアへのグルタミン酸放出の増強です。側坐核コアにおけるα-アミノ-3-ヒドロキシ-5-メチル-4-イソキサゾールプロピオン酸(AMPA)型グルタミン酸受容体の阻害、またはシナプス前GluR2自己受容体の活性化は、コカインおよび手がかり誘発性のコカイン探索の両方を阻害します。中脳皮質辺縁系回路内のドーパミン伝達も薬物プライミングによる再発に必要であり、内側前頭前野におけるドーパミンD1受容体の遮断は再燃を減少させます。可逆的な薬理学的失活研究により、薬物プライミングによる再燃には追加の脳領域が関与していることが示唆されています。これらには、腹側海馬支脚、腹側淡蒼球、中心扁桃体および基底外側扁桃体が含まれます。
依存症に関する神経科学研究のあらゆる分野からの収束的な証拠は、異なる薬物クラスの作用と結果が互いに異なる可能性があるという点を強調しています。一例として、ヘロインプライミングによるヘロイン探索の再燃の根底にある神経回路は、明確な要素と重複する要素の両方を持っています。コカインプライミングによる再燃と比較して、ヘロインプライミングによる再燃ではより拡散した回路が関与しているように見えます。なぜなら、複数の皮質および辺縁系構造の不活化がヘロイン探索の再燃を完全に消失させるからです。これらのヘロインに特異的な脳領域には、黒質、BNST、および背内側視床が含まれます。さらに、ドーパミンには異なる役割があります。側坐核におけるD1またはD2ドーパミン受容体の遮断が、ヘロインおよびコカインプライミングによる薬物探索の再燃を阻止することが示されています。
条件付け手がかり誘発性再発
条件付け手がかり誘発性の薬物探索再燃の動物モデルでは、いくつかの研究により、離脱期間後に薬物探索行動を駆動する薬物と手がかりの関連性の発達と維持に皮質線条体辺縁系経路が関与していることが示唆されています。特に注目されてきたのは扁桃体であり、これは食欲および負の強化因子に対する情動的に関連する刺激の学習における重要な構造として確立されています。研究により、基底外側扁桃体の恒久的な興奮毒性病変または一時的な薬理学的抑制は、毎日のコカイン自己投与中のコカイン摂取には影響を与えないものの、薬物自己投与中止後長期間にわたる薬物対をなす手がかりによって生じるコカイン探索の再燃を消失させることが判明しました。追加の研究では、条件付け手がかりによる再燃に対する扁桃体の調節がドーパミン依存性であることが示されています。扁桃体におけるドーパミンD1受容体の遮断は手がかり誘発性の再燃を阻止する一方、手がかり提示中に扁桃体におけるドーパミンシグナル伝達を増加させるとコカイン探索が強化されます。
前頭前野(前帯状皮質および前辺縁皮質)および線条体の離散的な下位領域も、条件付け手がかり誘発性の再燃に関与しています。背内側前頭前野、外側眼窩前頭皮質、または側坐核コアの薬理学的失活は、手がかり誘発性のコカイン探索を減弱させます。同様に、腹側淡蒼球の病変または不活化は薬物探索への再発を抑制します。手がかり誘発性再発の動物モデルにおける扁桃体、前頭前野、腹側淡蒼球、および側坐核コアの回路は、ヒトのデータと驚くべき相同性を示しています。コカイン依存症のヒト被験者における脳画像研究では、コカイン対をなす手がかりが扁桃体、皮質の前帯状領域、側坐核、および眼窩前頭皮質の代謝活性化を増加させることが示されています。
限定的ではありますが、ヒトにおける手がかり誘発性再発の神経回路に関する画像研究は、メタンフェタミン、アルコール、オピオイド、ニコチンを含む様々な乱用薬物において、皮質および辺縁系構造の脳活性化の重複パターンを概ね発見しています。げっ歯類モデルでは、扁桃体はヘロインおよびメタンフェタミン対をなす手がかり誘発性の再発の両方に必要です。しかし、ヘロイン対をなす手がかり再燃ではより拡散した回路が関与しており、これは動物モデルで最もよく解析できるメカニズムの違いを示唆しています。
ヒトでは、長期間の禁断後でも渇望と再発が生じることがあります。理由は不明ですが、薬物渇望は時間とともに増減します。渇望の時間的変動と再発の持続的な能力を説明するために、手がかり誘発性の薬物渇望が禁断期間中に時間とともに進行的に増加し、数ヶ月(6ヶ月以上)にわたって高く維持される可能性があるという仮説が立てられました。この効果はアルコール依存症の文脈で最初に記述され、「アルコール欠乏効果」と呼ばれました。より最近では、この効果はより広範に「薬物渇望の潜伏期間」として概念化され、薬物からの離脱後に生じる手がかり誘発性のコカインまたはヘロイン探索の時間依存的増加によってげっ歯類でモデル化できることが示されています。薬物探索の手がかり誘発性再燃に関与する(上記で議論された)多くの同じ脳領域も、薬物渇望の潜伏期間に寄与しています。離脱の最初の数日間で、不活性なシナプスの数が増加します。これらのシナプスはNMDA受容体は含むがAMPAグルタミン酸受容体を含まないため、通常のシナプス伝達条件下では活動していません。しかし、これらの不活性なシナプスはその後、高コンダクタンスのカルシウム透過性AMPAグルタミン酸受容体で「満たされ」、腹側線条体の中型有棘ニューロンにおけるグルタミン酸作動性シナプスの増強をもたらします。カルシウム透過性AMPA受容体の発現増加というこの発見は、渇望の潜伏期間に関連する最も堅牢な薬物誘発性適応の一つです。さらに、薬物離脱後1日または30日後の再燃試験で評価された薬物渇望が測定された場合、腹側内側前頭前野、側坐核コア、および扁桃体中心核で神経活動の増加が実証されています。
ストレス誘発性再発
ストレスは、薬物誤用とSUDのあらゆる側面で役割を果たしています。SUDを持つ人々は、長期間の禁断後であってもストレスに対する行動感受性が増加しており、これは再発に対する負の感情性およびハイパーカティフェイアの臨床的関連性を支持しています。定義上、ストレスとは、生物に適応を要求するあらゆる要求(ストレッサー)に対する非特異的な反応です。ストレッサーは通常、HPA軸を活性化して生理学的および感情的反応を生み出します。ストレスの生物学的効果は比較的固定されており客観的に測定可能ですが、感情的効果はストレッサーに対処する個人の能力の認識に依存するため、より主観的です。ストレスの一般的な概念は、それが回避されるべき負の、うつ病様の感情(無快感症、不安、易刺激性、圧倒される感覚)の集合体であるというものです。ただし、ストレッサーとして適格と思われる刺激が、ポジティブまたは興奮するものとして経験されることもあります(例:新しい仕事、スカイダイビング)。SUD患者を対象とした対照実験室研究では、薬物渇望がストレッサーによって誘発される可能性があり、このストレス誘発性反応が再発を予測することが示されています。同じストレッサーが一方の個人には快楽を引き起こし、他方には嫌悪を引き起こす可能性があるという事実は、依存症治療の万能薬として包括的な「抗ストレス」薬理療法を開発することを非常に困難にしています。
薬物プライミングまたは条件付け手がかり誘発性の薬物探索の再燃に必要な回路の一部は、前辺縁皮質および側坐核、ならびに広範な扁桃体内の構造を含む、ストレス誘発性の再燃にも必要です。BNSTおよび扁桃体中心核(ただし基底外側扁桃体ではない)の不活化は、ストレス誘発性の再燃を減弱させます。間欠的な足底電気ショック誘発性の再燃については、研究により、VTAにおけるCRFとグルタミン酸の役割、および扁桃体中心核からBNSTへのCRF投射の役割が示されています。CRFの中心部への注入は再燃を生み出す一方、CRF受容体およびイオノトロピックグルタミン酸受容体拮抗薬は、ノルアドレナリンα2受容体作動薬と同様に、コカインおよびヘロイン探索のストレス誘発性再燃を阻害します。
ストレス反応において役割を果たすことが知られている他の多数の神経伝達物質システムも、ストレス誘発性の再発に寄与している可能性があります。例えば、離脱中および遷延性離脱中のストレスに対する脆弱性の増強は、部分的に中脳皮質辺縁系における低ドーパミン状態に起因する可能性があります。薬物依存症および初期の薬物離脱は、側坐核などの辺縁系領域におけるドーパミンレベルおよびドーパミン受容体の減少と関連付けられています。離脱中の持続性ドーパミンレベルの低下は、ストレッサーに対する位相性ドーパミンシグナルへのより良いコントラスト、または「信号対雑音比」を提供する可能性があります。前述のように、神経ペプチドダイノルフィンは慢性薬物投与により増加し、ドーパミン作動性神経終末のKORに作用してドーパミン放出を減少させます。これは、慢性的に上昇したダイノルフィン発現と放出が、薬物離脱誘発性の低ドーパミン状態とストレス感受性の増加に寄与する可能性があることを示唆しています。これと一致して、選択的拮抗薬nor-BNIによるVTAにおけるKORの遮断は、ラットにおけるスイムストレス誘発性のコカイン探索再燃を減少させます。条件付け手がかり、薬物プライミング、およびストレスによって生じる薬物探索行動の再燃のための共有および明確な神経回路の要約模式図を図1.31-6に示します。
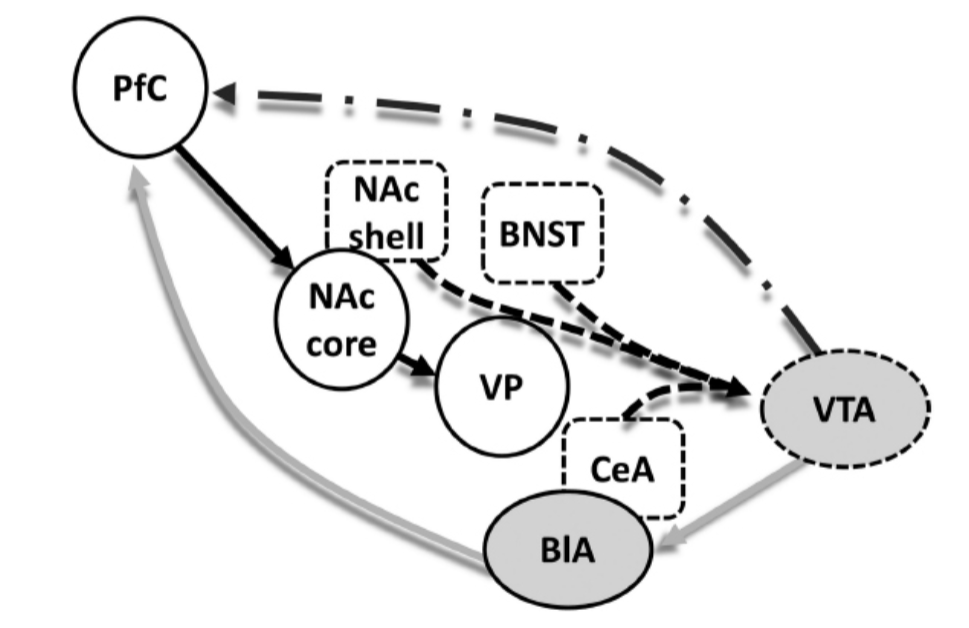
図1.31-6. 薬物探索を媒介する神経回路。
前頭前野から側坐核コア、腹側淡蒼球への直列投射(白丸)は、広範な扁桃体回路内(白い破線ボックス)、薬物関連手がかり(灰色の楕円)、または薬物自体(腹側被蓋野から前頭前野への一点鎖線はドーパミン放出の増加を示す)によって開始されるストレス誘発性薬物探索の最終共通経路です。PfC, 前頭前野; NAc, 側坐核; VP, 腹側淡蒼球; BNST, 分界条床核; CeA, 扁桃体中心核; BLA, 基底外側扁桃体; VTA, 腹側被蓋野。
依存症の細胞および分子基盤
SUDを、解毒後も持続し、薬物使用の継続、渇望、再発の原因となる脳の適応を伴う再発性CNS疾患として定義するには、そのような神経適応を特定し、理解することが必要です。これは、乱用薬物への慢性曝露が、薬物の種類と投与経路、研究される脳領域、発達歴、生物学的性別などによって異なる、多数の細胞および分子適応を引き起こすため、困難であることが証明されています。現在の課題は、異なる薬物クラス(例:精神刺激薬とオピオイド)が、類似の行動を生み出す一方で、一見異なる分子および細胞適応を生み出すメカニズムを理解することです。以下に、薬物誘発性神経適応のいくつかの代表的な例と、その機能的意義に関する現在の理論をいくつか挙げます。これは、非常に高い利害関係を持つ急速に変化する研究分野です。効果的なSUD治療法の開発がその利害関係に当たります。
遺伝子発現
薬物誘発性の分子変化を調べた研究の大部分は、中脳皮質辺縁系(VTA、側坐核、前頭前野)と、 altered dopamine signaling(ドーパミンシグナル伝達の変化)の結果に焦点を当ててきました。上述したように、すべての乱用薬物の共通の初期作用は、側坐核における細胞外ドーパミンレベルの増加です。ドーパミンはD1またはD2様Gタンパク質共役型ドーパミン受容体に結合して活性化し、それぞれアデニル酸シクラーゼと環状アデノシン一リン酸(cAMP)産生の刺激または抑制につながります。分子セカンドメッセンジャーとして、cAMPは、cAMP依存性プロテインキナーゼA(PKA)の活性化と、それに続く転写因子であるcAMP応答要素結合タンパク質(CREB)の活性化部位のリン酸化を含む、複数の細胞内効果を持っています(図1.31-7)。そのため、ほとんどの乱用薬物の信頼できる急性効果は、側坐核における穏やかなD1受容体媒介性CREBリン酸化です。さらに重要なことは、SUDの発症に関して、乱用薬物の慢性投与は、cAMP-PKAシグナル伝達経路に代償的適応を生み出すことです。コカイン、アンフェタミン、またはオピオイドへの反復曝露は、側坐核におけるCREB活性を有意に誘導しますが、アルコールとニコチンはこの領域におけるCREBリン酸化を減少させます。薬物誘発性のCREB活性の調節は、側坐核に限定されません。例えば、急性モルヒネは抑制性μ-オピオイド受容体に結合し、オピオイドの身体的依存と離脱にとって重要な脳領域である青斑核におけるCREBリン酸化を阻害します。この阻害は、アデニル酸シクラーゼ媒介性cAMP産生の代償的アップレギュレーションとPKAの活性化により、慢性モルヒネ曝露により耐性を生じます。モルヒネ離脱時、このアップレギュレートされたcAMP/PKA経路はCREB活性化の急増をもたらし、これは離脱症状に寄与すると考えられています。最後に、いくつかの乱用薬物の慢性投与がVTAでCREBを活性化するという証拠があり、これはVTAドーパミンニューロンのドーパミン合成と興奮性に直接影響を与えます。CREBは、VTAにおけるドーパミン生合成の律速酵素であるチロシンヒドロキシラーゼ(TH)の発現を誘導します。VTAにおけるTH遺伝子発現の増加にもかかわらず、特定の実験条件下では、側坐核のVTA神経終末におけるTHタンパク質レベルおよび/または活性の減少が報告されています。THタンパク質レベルの減少は、慢性薬物誘発性低ドーパミン状態と負の感情状態の出現を媒介する可能性があります。
CREBリン酸化は数分オーダーの一過性の効果ですが、CREBの繰り返し短い活性化は、ニューロンのトランスクリプトームに多数の変化を引き起こし、それが個々の細胞およびそれらが埋め込まれている回路の生理機能に重大な変化をもたらします。SUDにおいて重要な役割を果たす可能性のあるCREB制御遺伝子のいくつかの例には、c-Fosなどの他の転写因子、細胞内メッセンジャー(例:アデニル酸シクラーゼVI. VIII)、神経伝達物質生合成酵素(例:TH)、ペプチド神経修飾物質(例:CRFおよびソマトスタチン)、成長因子(例:脳由来神経栄養因子[BDNF])、オピオイドペプチド(例:ダイノルフィンおよびエンケファリン)、および神経伝達物質受容体サブユニット(例:GluR1)が含まれます(図1.31-7参照)。側坐核における慢性薬物誘発性CREB活性化の行動効果は、薬物間で類似する傾向があります。側坐核におけるCREB活性の増加は、コカイン、オピオイド、アルコールに対する行動反応を減少させる一方、CREB活性の減少はそのような反応を増加させます。この多くの実験システムで様々な方法で観察されている知見は、側坐核CREB活性化が薬物の継続的な存在に対抗するために動員される分子拮抗プロセスであるという仮説につながりました。この仮説を裏付けるように、CREB誘発性ダイノルフィンはVTAドーパミンニューロンとその神経終末のKORを活性化し、ドーパミン作動性トーンの減少と、薬物の存在下での薬物報酬への対抗、または薬物の不在下での負の感情状態の産生(すなわち離脱)をもたらします。
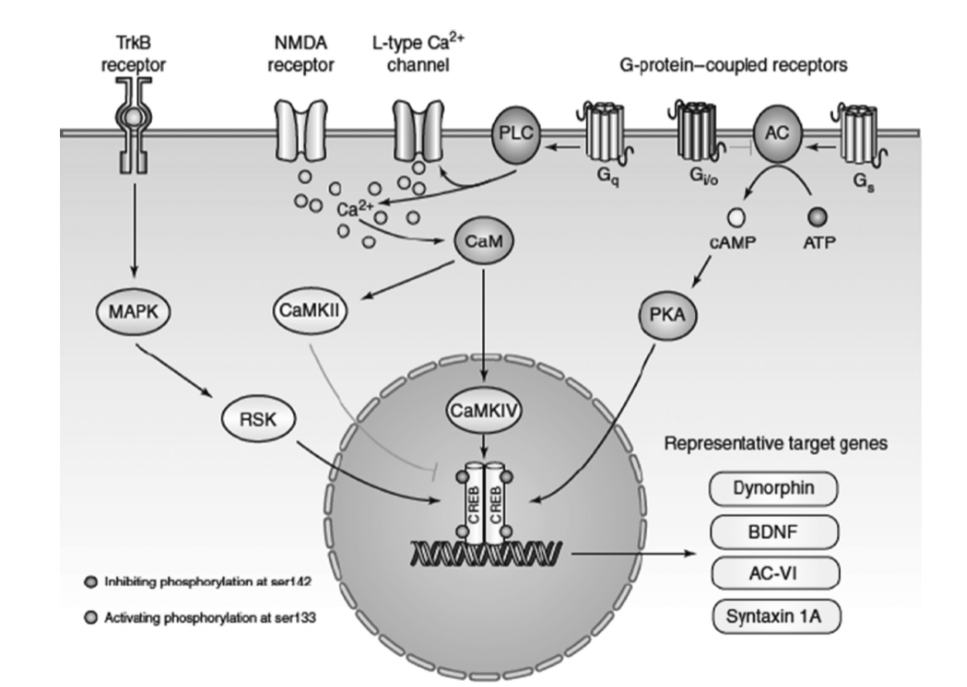
図1.31-7. 細胞外シグナルがCREBを介して遺伝子転写に影響を与える方法の簡略図。
CREBのser133でのリン酸化は、その転写活性と標的遺伝子発現を増加させます。CREB活性は、CREBのser142でのリン酸化によって減弱される可能性があります。側坐核(NAc)内では、Gαs共役受容体(例:ドーパミンD1)を発現するニューロンはアデニル酸シクラーゼ(AC)を活性化し、Gαi/o共役受容体(例:ドーパミンD2)を発現するニューロンはACを抑制します。NAcにおける薬物誘発性のドーパミン増加への曝露は、MAPKおよびカルシウム(Ca2+)感受性シグナル伝達経路の活性化も引き起こす可能性があります。明確にするため、セカンドメッセンジャー間のクロストークは含まれていません。黒線は活性化を意味し、灰色線は抑制を意味します。(Muschamp JW, Carlezon WA, Jr. Roles of nucleus accumbens CREB and dynorphin in dysregulation of motivation. Cold Spring Harb Perspect Med. 2013;3(2):a012005.O Cold Spring Harbor Laboratory Press. doi:10.1101/cshperspect.a012005より許可を得て転載。)
CREB活性化に加えて、乱用薬物は、側坐核におけるFosタンパク質ファミリー(c-fos、ΔFosB、Fra-1、Fra-2)のメンバーやNAC-1を含む他の転写因子を活性化させます。これらの遺伝子産物が急性薬物報酬に直接関与している可能性は低いと考えられます。なぜなら、これはドーパミンやオピオイド受容体刺激に関連するより即時的なシグナル伝達イベントに依存するからです。
ΔFosBは、FosBの非常に安定した形態であり、実質的にすべてのクラスの乱用薬物の反復投与により時間とともに蓄積することが示されています。ΔFosBが活性化された動物は、モルヒネとコカインの報酬効果に対する過剰な感受性を示すことが示されています。このことから、ΔFosBは依存症の状態を開始し、維持するのに役立つ持続的な分子「スイッチ」である可能性があるという仮説が導かれました。CREBと同様に、ΔFosB自体は細胞機能に寄与しませんが、神経可塑性に関与するタンパク質をコードする多数の遺伝子の転写を促進します。総合すると、乱用薬物が遺伝子発現をどのように調節するかという現在の理解は、主に単一の薬物クラス(例:精神刺激薬またはオピオイド)に焦点を当てた研究から得られています。コカインおよびヘロイン使用障害を持つ人々の剖検研究では、側坐核で調査された約39,000の遺伝子転写産物のうち、コカインおよびヘロインの両方の使用者で発現が変化したのはわずか25遺伝子でした。これらの遺伝子の約半分では、薬物が発現に対して逆の作用をもたらしました。
乱用薬物が遺伝子発現をどのように調節するかという最後の例は、乱用薬物がVTA、側坐核シェル、および扁桃体でBDNFを上方制御するという発見であり、そこでは「プロ依存性」調節因子として作用すると考えられています。BDNFはシナプス前軸索の分岐と組織化、ならびにシナプス後樹状突起の樹状突起形成、数、サイズ、運動性を促進し、シナプスタンパク質の合成を強化します。BDNFは急性薬物投与によって増加しますが、コカイン自己投与からの離脱中、側坐核におけるBDNFタンパク質レベルは増加し続け、離脱約30日後に最大レベルが観察されます。BDNFは何ヶ月も上昇したままである可能性があります。BDNF蓄積の時間パターンは、薬物渇望の潜伏期間という現象(条件付け手がかり誘発性再発で上記で議論されたように)と一致し、VTA内または側坐核シェルへのBDNF注射は、離脱後のコカイン探索の遅延性かつ長期的な増加を引き起こします。しかし、前頭前野から側坐核へのBDNF投射がコカイン探索への脆弱性を減少させることが示されています。これは、タンパク質やその他の調節因子の行動効果が、それらが作用する神経回路にどのように依存するかを示すもう一つの重要な例です。
ニューロン形態とシナプス可塑性
反復的な薬物曝露後の中脳皮質辺縁系経路におけるドーパミンおよびオピオイド受容体媒介性の遺伝子発現の変化に加えて、薬物使用から依存症への移行は、皮質回路の持続的な再構築を伴います。薬物誘発性の構造可塑性には、細胞体のサイズの変化、および樹状突起の樹状突起形成または棘の形態の変化が含まれます。観察される最も一貫性があり認識可能な細胞適応は、樹状突起棘密度の形態学的変化です。これらの変化は、おそらく細胞骨格調節タンパク質をコードする遺伝子の薬物誘発性調節によるものであり、Homer 1およびシナプス後密度95(PSD95)のレベルの低下が含まれ、これらは両方ともシナプス後アクチン細胞骨格と関連する足場タンパク質です。さらに、モルヒネとコカインは、アクチン細胞骨格を調節する小型GTPaseであるRhoA、Rac1、および細胞分裂周期42(Cdc42)を減少させることが示されています。
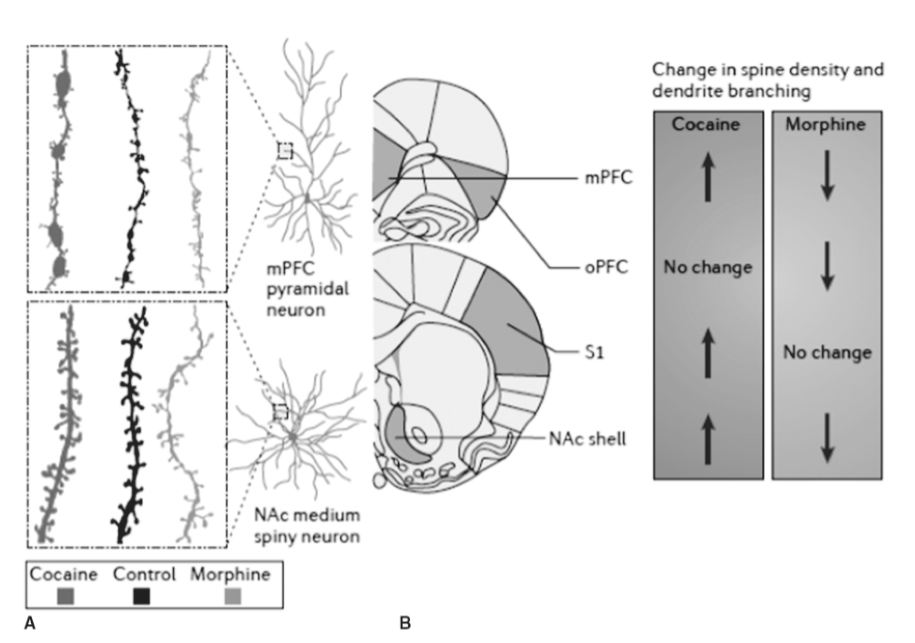
図1.31-8. モルヒネとコカインが側坐核(NAc)および内側前頭前野(mPFC)の構造的神経可塑性に対して逆の効果を持つこと。
A: ラットのグループは、数週間にわたりモルヒネまたはコカインを静脈内自己投与するように訓練されました。対照グループは、同じ期間、毎日ビヒクルを静脈内投与されました。薬物からの離脱1ヶ月後、ラットの脳はゴルジ染色法を用いて処理されました。コカインに曝露されたラットは、NAc中型有棘ニューロンとmPFC錐体細胞の両方で、樹状突起の分岐と棘密度の増加を示しました。対照的に、モルヒネに曝露されたラットは、これらの脳領域で樹状突起の分岐と棘密度の両方が減少していました。B: コカインまたはモルヒネへの曝露後に生じる棘密度および樹状突起分岐の変化を対照と比較してまとめたもの。コカインとモルヒネの効果の間の乖離は、眼窩前頭皮質(oPFC)および一次体性感覚皮質(S1)でも観察されました。(Badiani A, Belin D, Epstein D, Calu D, Shaham Y. Opiate versus psychostimulant addiction: the differ-ences do matter. Nat Rev Neurosci. 2011;12:685-700, Springer Nature. doi: 10.1038/nrn3104より転載。)
依存症研究における現在のパラドックスは、オピオイドが側坐核、内側前頭前野、および海馬錐体細胞のニューロンにおける樹状突起棘の数と複雑性を減少させる一方、精神刺激薬はそれを増加させるという一般化にあります(図1.31-8)。同様に、オピオイドはVTAドーパミン作動性ニューロンの体細胞サイズを減少させる一方、精神刺激薬はそれを増加させます。これらの変化は、最後の薬物曝露後2週間以内に正常化するように見えます。オピオイドと精神刺激薬のこれらの異なる細胞効果を調和させるための一つの仮説は、モルヒネとコカインの反復投与の両方がアクチンサイクリングを増加させるという発見を含みます。これは理論的に棘密度の増加または減少につながる可能性がありますが、より重要なのは、薬物誘発性のグルタミン酸放出の変化に対する応答の可塑性が大きいことと関連していることです。
異なる薬物クラスがニューロンの形態とシナプス強度に対して明らかに逆の効果を持つにもかかわらず、薬物クラスとは独立して生じる神経適応が、薬物クラスを超えて存在するSUDの中心的要素にとって特に重要であるという暗黙の前提がありました。再発はSUDの中心的要素であり、薬物クラスに関係なく、手がかり誘発性の再燃が、側坐核のコア、特にD1受容体発現ニューロンにおけるグルタミン酸作動性シナプスの急速で一過性のシナプス増強を伴うことが示されています。加えて、樹状突起棘頭の拡大とAMPAを介するグルタミン酸作動性伝達の増加が観察されます。さらに、細胞外マトリックスは、神経伝達修飾因子に富んだ環境を構成しており、その多くが依存症に関与している可能性があります。一例として、**マトリックスメタロプロテイナーゼ(MMP)**は、シナプス可塑性を強力に調節する細胞外プロテアーゼのファミリーです。乱用薬物および薬物探索の再燃は、MMP活性を急速に誘導し、それに続く樹状突起棘頭の拡大と側坐核コアにおけるシナプス強度の増加をもたらします。同様に、MMP活性を阻害すると薬物探索への再燃が阻止されます。最後に、比較的consistentな発見は、薬物探索が側坐核におけるグルタミン酸放出の増加と関連していることです。増強されたグルタミン酸放出の根底にあるメカニズムには、グリアにおけるシスチン-グルタミン酸交換のダウンレギュレーション、シナプス前代謝性グルタミン酸受容体(mGluRs)を介するシグナル伝達の減少、およびグルタミン酸トランスポーターによるグルタミン酸の除去の減少が含まれます。
エピジェネティクス
エピジェネティクスは広義に、DNA配列の変化なしに動物の生涯にわたって遺伝子発現の変化が達成される一連の生化学的プロセスと定義できます。エピジェネティクスは、経験依存的なニューロンの発達と可塑性、および依存症関連行動の根底にある持続的な構造的および機能的変化を生み出すために、環境と遺伝子が相互作用する手段です。DNAはクロマチンに組織化されており、クロマチンの基本的な単位はヌクレオソームであり、これはヒストンのコアグループに巻き付けられたDNAから構成されています。エピジェネティックなメカニズムは、インターヌクレオソーム間隔とそれらが凝縮される程度を制御し、これは遺伝子活性の決定要因となります。ヘテロクロマチンは凝縮され不活性化された状態を指し、遺伝子転写を許容しません。一方、ユークロマチンは活性化され開かれた状態を指し、個々の遺伝子の転写を許容します。エピジェネティック制御には、ヒストン修飾(例:アセチル化とメチル化)、DNAメチル化、および制御的非コードRNAの3つの主要なタイプがあります。
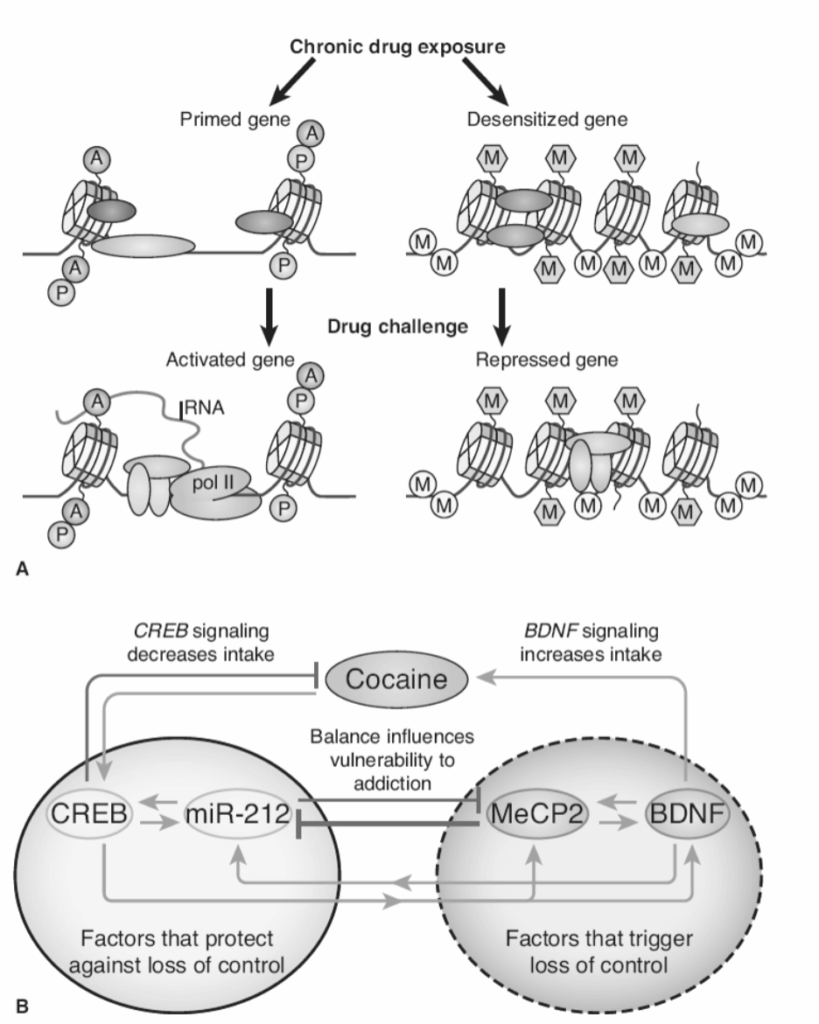
図1.31-9. A: 遺伝子プライミングと脱感作における急性および慢性薬物効果に関与するエピジェネティックメカニズム。
多くのエピジェネティック変化は潜在的であり、定常状態のmRNAレベルの安定した変化には反映されないことを意味します。代わりに、そのような変化はクロマチン構造を変化させ、以前の慢性薬物曝露によって誘発されたエピジェネティック修飾に基づいて、後の薬物刺激が特定の遺伝子をより大きな(プライミングされた)またはより小さな(脱感作された)程度で誘導するようにします。A, アセチル化; M, メチル化; P, リン酸化; pol II, RNAポリメラーゼII。(Aは、Robison AJ, Nestler EJ. Transcriptional and epigenetic mechanisms of addiction. Nat Rev Neuro-sci. 2011;12:632-637, Springer Nature. doi:10.1038/nrn3111より。)B: マイクロRNA 212(miR-212)、cAMP応答要素結合タンパク質(CREB)、メチルCpG結合タンパク質2(MeCP2)、および脳由来神経栄養因子(BDNF)間の複雑な相互作用と、コカイン摂取に対するそれらの推定される効果。
黒線で囲まれた円は、CREBシグナル伝達がコカイン摂取の段階的増加の発達から保護することを示唆する一方、点線で囲まれた円は、MeCP2-BDNFシグナル伝達が摂取の段階的増加を促進することを示唆します。薄い灰色の矢印は刺激的関係を示し、濃い灰色の線は抑制的関係を示します。コカインはCREBとMeCP2-BDNFシグナル伝達の両方を活性化し、miR-212によって調整されるこれら2つの経路間のバランスは、拡張アクセスラットにおけるコカイン摂取の段階的増加、およびおそらくコカイン依存症への脆弱性を調節すると考えられます。(Bは、Jonkman S, Kenny PJ. Molecular, cellu-lar, and structural mechanisms of cocaine addiction: A key role for microRNAs. Neuro-psychopharmacology. 2013;38:198-211, Springer Nature. doi:10.1038/npp.2012.120より。)
エピジェネティクスは依存症において主要な役割を果たす可能性が高いです。乱用薬物やその他の環境的な損傷への反復的な曝露は、幼少期(または成人期)にエピジェネティックプロセスを活性化する可能性があります。これらのエピジェネティックプロセスは、特定の遺伝子または遺伝子のセットに作用し、遺伝子発現の安定した変化、または脆弱な個人で依存症につながる可能性のある他の遺伝子の誘導性の変化を引き起こします(図1.31-9A)。また、薬物やその他の環境的な損傷が配偶子にエピジェネティックな変化を生み出し、それが子孫に受け継がれてSUDへの脆弱性を高める可能性もあります。依存症への脆弱性の世代間エピジェネティック遺伝というこの考えを支持する証拠が増加していますが、まだ議論の余地があります。そこで、以下にエピジェネティック変化の2つの顕著な例を説明します。
ヒストンアセチル化
**ヒストンアセチルトランスフェラーゼ(HAT)とデアセチラーゼ(HDAC)**はそれぞれ、ヒストンのアセチル化と脱アセチル化を触媒します。アセチル化はクロマチンの脱凝縮を促進し、一般的に遺伝子活性を増加させます。ヒストンアセチル化に関する依存症研究の大部分は、側坐核におけるアセチル化ヒストンの総細胞レベルを増加させる精神刺激薬で行われてきました。c-Fos遺伝子プロモーターは薬物治療後短期間アセチル化されますが、慢性的な変化は観察されません。これは、c-Fos mRNAの急速なオンオフ発現パターンと一致しています。対照的に、BDNFプロモーターは慢性コカイン後のみアセチル化され、慢性コカイン後および離脱中にのみBDNFタンパク質が蓄積することと一致しています。しかし、コカインに反応してヒストンアセチル化が変化するほとんどの遺伝子は、過剰または低アセチル化で予想されるmRNA発現の変化を示しません。さらに、ヒストンアセチル化の行動効果を解析することは困難です。なぜなら、各遺伝子プロモーターにはエピジェネティック制御が生じる複数の部位があるからです。
マイクロRNA
**マイクロRNA(miRNA)**は、標的mRNAに結合し、その翻訳を阻害するか分解を誘導する、小さな非コードRNA転写産物(約22ヌクレオチド)です。現在までに、数百のmiRNAが特定されており、各miRNAは何百から何千ものmRNA転写産物を標的とする可能性があります。miRNA miR-212に焦点を当てた一連の研究(図1.31-9B)では、ラットにおけるコカイン自己投与への拡張アクセスが線条体におけるmiR-212レベルを増加させることが示されました。研究者によって制御された線条体におけるmiR-212の過剰発現は、特に薬物への拡張アクセスを与えられたラットにおいて、コカイン自己投与への動機付けを減少させましたが、薬物アクセスが制限されたラットにおけるコカイン自己投与には影響を与えませんでした。CREBはmiR-212の発現を増加させ、miR-212自体が線条体におけるCREB活性を劇的に増加させる可能性があります。BDNFはCREB標的遺伝子ですが(上記参照)、miR-212の上昇は実際には線条体におけるBDNF発現を抑制します。総合すると、エピジェネティック調節因子であるmiR-212は、慢性コカイン自己投与によって増加し、CREBを活性化し、BDNFを抑制します。これらの発見は、miR-212がコカイン依存症の発症から保護する可能性があることを示唆しています。
物質使用障害における性差
人間では、SUDのほとんどあらゆる側面で数多くの性差が見られます(表1.31-4参照)。ほとんどの薬物において、男性は女性と比較して一貫して使用、誤用、依存の割合が高く、全体的なオッズ比は2:1(男性:女性)です。しかし、これらの差は減少傾向にあります。例えば、女性のアルコール誤用率は急速に男性の率に近づいています。これは、SUDにおける人口レベルの性差の多くが、生物学的性質というよりも文化的性質のものである可能性を示唆しています。とはいえ、臨床および前臨床研究は、性腺ホルモンとストレスおよび中脳辺縁系ドーパミンシステムとの相互作用に関連する有意な性差を明らかにしています。蓄積された証拠は、女性が男性よりも早く物質使用からSUDへと進行する**「テレスコーピング」**と呼ばれる現象を示唆しています。SUDの動物モデルでは、薬物感受性および自己投与行動に性差が見られます。繰り返しの薬物曝露、特に精神刺激薬は、男性と比較して女性において誘因感作をより大きく増強します。一般に、女性は、依存サイクルの各段階(獲得、維持、エスカレーション、再発)において、精神刺激薬、オピオイド、ニコチンの強化効果に対して男性よりも脆弱です。
コカイン使用における女性の主観的効果:神経過敏
- コカイン
- 所見: 女性は、コカイン使用時に神経過敏をより強く感じやすいとされています。
- アンフェタミン:
- 女性は、卵胞期(生理周期の一部)に多幸感やハイな感覚をより強く感じやすいとされています。
- エストロゲンレベルが高いと、女性はアンフェタミンによる快い刺激をより強く感じるようです。
- コカイン:
- 総使用量に関しては、男女間に有意な差は見られません。
- 女性は、コカインに関連する手がかりへの反応性が男性よりも高い傾向があります。
- 禁断期間中の薬物への渇望も、女性の方が男性よりも強いと報告されています。
- オピオイド:
- 総使用量においても、使用パターンにおいても、男女間に性差は見られません。
- 禁断症状についても、性差は観察されていません。
このデータは、薬物使用の全体的な割合に大きな差がなくても、特定の薬物に対する主観的な体験、渇望の強さ、そして再発の可能性は、性差、特に女性のホルモン変動によって影響を受ける可能性があることを示唆しています。

物質使用およびSUDにおける性差の生物学的メカニズム
物質使用および物質使用障害(SUD)における性差の根底にある生物学的メカニズムは、いまだ解明されつつあります。SUDの発症に寄与するポジティブおよびネガティブな強化プロセスに関わる基本的な神経システムは、男女間で類似していますが、これらのシステムの組織と結合性には性差が報告されています。性がSUDにどのように影響するかを考える際には、性差が行動レベルおよび/または神経レベルで生じうることを念頭に置くことが重要です。SUDにおける性の役割の厳密な検討は比較的新しいため、現在の知識にはまだ多くのギャップがあります。薬物の種類、実験パラダイム、動物種、および発情周期などの要因が、乱用薬物に対する行動的および神経生物学的反応に寄与することが明らかになっています。そのため、現在利用可能なデータの多くは非常にばらつきがあります。以下に、物質使用および依存症における性差の根底にあるとされるメカニズムの、比較的確固たる2つの例を挙げます。
性腺ホルモンの活性化効果
前臨床研究と臨床研究の両方からの証拠は、女性の生殖周期を通じて(図1.31-10)、性腺ホルモン、特にエストロゲンとプロゲステロンの変動が、薬物への反応における性差に重要な役割を果たすことを示しています。例えば、アンフェタミンのいくつかの強化効果(多幸感やエネルギー増加など)は、女性の卵胞期において黄体期と比較して増強され、エストロゲンレベルと正に相関しています。これと一致して、卵胞期における外因性エストロゲン投与は、女性における精神刺激薬の主観的効果を高めます。エストロゲンの増強効果とは対照的に、プロゲステロンレベルは精神刺激薬の主観的効果と負に相関しています。さらに、卵胞期における外因性プロゲステロン投与は、コカインの多くのポジティブな主観的効果を減少させます。
動物モデルを使用することで、性腺ホルモンの行動への影響をより正確に調べることができます。なぜなら、性腺摘出術によってホルモンの供給源を排除し、その後、投与量とタイミングを実験的に制御しながらホルモンを再導入できるからです。これらの方法を用いて、卵巣摘出がコカイン自己投与を減少させ、外因性エストロゲン治療が卵巣摘出ラットにおけるコカイン、モルヒネ、ヘロイン自己投与の獲得を促進するのに十分であることが示されています。興味深いことに、雄ラットにおけるコカイン自己投与の獲得には、去勢による影響はありません。
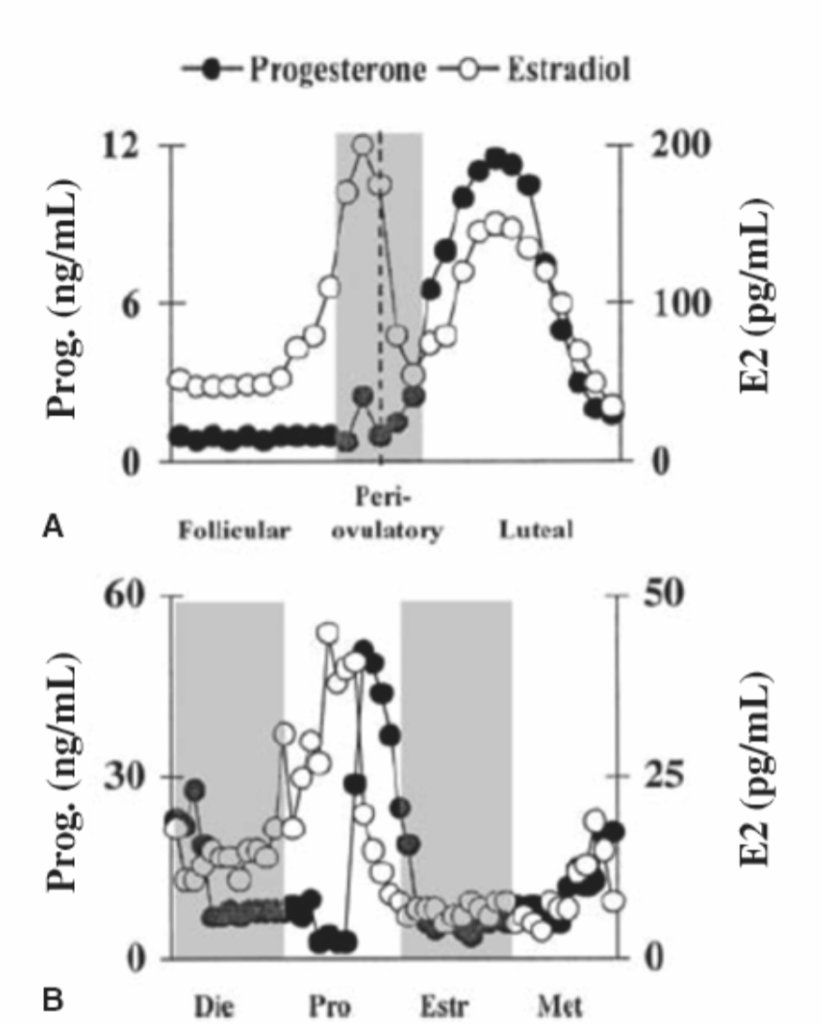
図1.31-10. 女性の生殖周期における性腺ホルモン変動。
A: ヒト月経周期における排卵前黄体形成ホルモン(LH)サージからの日数関数としてのエストロゲン(E2)とプロゲステロン(Prog)のレベルの変化。影付きの棒は、排卵期を卵胞期と黄体期から分離しています。B: ラットの発情周期の各段階におけるエストロゲンとプロゲステロンのレベルの変化。影付きの棒は、各段階の開始と終了を識別するために、連続する発情周期の段階である発情休止期(DIE)、発情前期(PRO)、発情期(ESTR)、および発情後期(MET)を分離しています。(Lynch WJ, Roth ME, Carroll ME. Biological basis of sex differences in drug abuse: preclinical and clinical studies. Psychopharmacology. 2002;164:121-137, Springer Nature. doi:10.1007/s00213-002-1183-2より。)
ドーパミンシグナル伝達における性差
依存症における性差の根底にあるメカニズムの可能性を示す2つ目の例として、中脳ドーパミンニューロンの数と機能が性的二形性を示すことが報告されています。例えば、女性は男性と比較してドーパミン合成およびドーパミントランスポーター(DAT)を介した再取り込みの能力が高いと報告されています。
性腺ホルモンは、側坐核と背側線条体におけるドーパミン終末の密度およびドーパミンニューロンの発火率を調節することができます。ドーパミン終末の密度は、基礎的なドーパミンレベルに影響を与え、これは女性では生殖周期を通じて変動するものの、男性では比較的安定していることが示されています。例えば、雌ラットは発情周期中により高い発火率とより多くのバースト発火をドーパミンニューロンで示します。発情周期に関係なく、女性は男性と比較して、基礎的なドーパミン放出およびコカイン刺激によるドーパミン放出と再取り込みが大きいという証拠もあります。
現在の治療法
SUDの治療は、解毒期、初期回復期、再発予防期の3段階で構成されます。解毒後、初期回復期の目標は、外部または内部の手がかりによって誘発される渇望に耐えることを学び、再発を防ぐのに役立つ新しい行動パターンを学ぶことです。再発予防治療の目標は、個人が中毒行動を新しい健康的な行動に置き換える長期的な戦略を開発することです。治療法には、薬理学的、行動学的、社会的、および/または認知的なものがあります。臨床および前臨床研究者の間では、最も効果的な治療法は、SUDの根底にある基本的な神経メカニズムの理解から得られる科学的証拠に基づいているという一般的な合意があります。
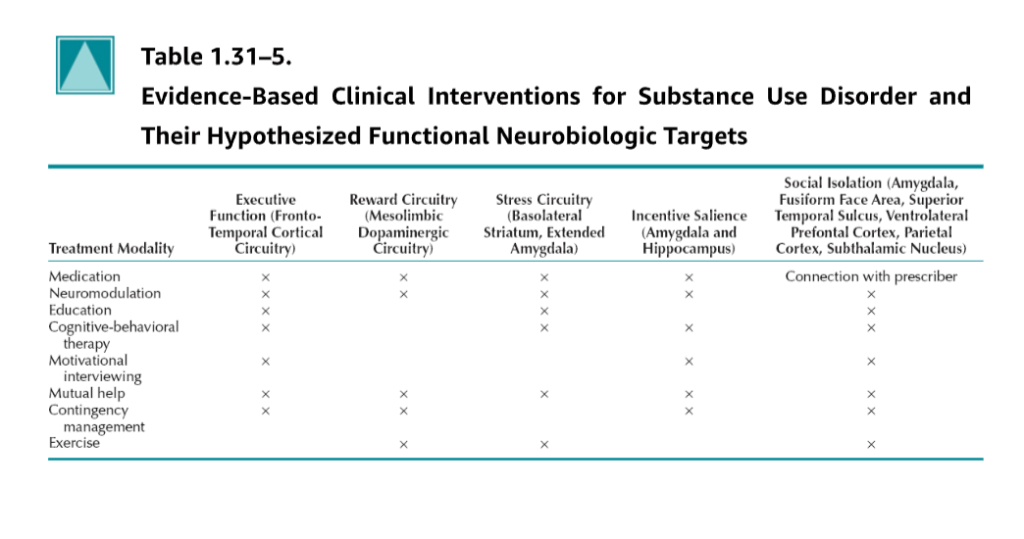
エビデンスに基づく臨床介入は、SUD患者の関与プロセスおよび早期回復治療中に標的とされる神経生物学的基質に従って、効果的な介入として理解できます(表1.31-5)。例えば、薬物介入は、慢性的な物質曝露および生理的依存と離脱症候群の発症に関連するアロスタシス状態を改善するように設計されています。そのため、これらのシステムの安定化には、離脱症状、物質への渇望、および早期禁断に関連する過覚醒の改善が含まれます。これは臨床的に、実行機能と衝動制御、学習と注意、ストレスと手がかり反応性の低下、社会的正常化における個人の能力の向上につながります。
心理社会的介入も、その構造の構成要素に基づいて同様に概念化できます(表1.31-5参照)。心理社会的介入には、SUDとその治療に関する教育、健康とウェルネスの要素としての運動プログラムへのアクセス、禁断を支援することを目的とした自助グループ支援プログラム(例:アルコホーリクス・アノニマスとして設立された12ステップの回復モデル)などの地域ベースの介入と、動機づけ面接、認知行動再発予防、ポジティブ強化偶発性管理などの訓練された臨床医によって提供される専門的介入の両方が含まれます。例えば、教育は、SUDのリスク要因について個人に教え、また物質使用を控えることで抑制される可能性のある脳疾患としてのSUDの基本的な理解を提供する予防および治療モダリティです。そのため、主に個人が健康的な選択をし、健康的なソーシャルネットワークを促進し、ストレスに対処する手段として物質を使用することを避けるのに役立ちます。これは、報酬追求行動や関連する誘因顕著性を変化させるにはあまり影響がなく、また離脱症候群を安定させるのにも役立ちません。動機づけ面接として知られる関与介入は、個人が自分の目標、価値観、現在の動機付けられた行動パターンをよりよく定義できるように支援するための、訓練された対話プロセスを指します。目標は、個人が目標に合致する動機付けられた行動に焦点を当て、個人的な目標や価値観と矛盾する結果をもたらす動機付けられた行動(物質誤用など)を減らすのを支援することです。動機づけ面接は、個人が変化を計画するのに成功的に関与するかもしれませんが、それ自体で主観的な報酬駆動行動および/またはストレス軽減を大きく変化させる可能性は低いため、動機づけ面接は、禁断回復期の治療中にこれらの側面を変化させることをより具体的に目的とした、認知行動再発予防や偶発性管理などの他の療法への関与を支援するプラットフォームとして最適に機能します。興味深いことに、自助グループ支援は、「人、場所、物」などの依存症の手がかりを理解し、物質使用の機会を避け、ストレス軽減と自然な報酬のためのより健康的な代替手段を開発し、計画された回復と有意義な人生の追求に有意義な社会的つながりを統合するように個人を訓練する社会的に促進されたシステムであるという性質上、回復において最も広範な神経基盤の「カバレッジ」を提供する可能性があります。
脳回路における神経活動を変化させる介入と定義されるニューロモジュレーションは、SUDの有望な治療アプローチとして浮上しています。ニューロモジュレーションツールには、脳深部刺激療法(DBS)などの侵襲的アプローチと、経頭蓋磁気刺激(TMS)や経頭蓋直流電気刺激(tDCS)などの非侵襲的アプローチが含まれます。TMSは現在、ニコチン使用障害の治療薬としてFDAの承認を受けています。
以下に、オピオイドおよび精神刺激剤SUDの2つの臨床例と、現在利用可能な臨床的に推奨される治療法を示します。
現在の治療法:臨床事例
事例1:ヘロイン使用障害の若い女性(23歳)
状況:
23歳の未婚女性、子供なし。小売店のパートタイム従業員で、週末はダンサーとして働く。静脈注射によるヘロイン使用障害の初回治療のため来院。幼少期および成人期の性的トラウマの重大な既往あり。14歳で喫煙、友人と断続的な飲酒、大麻の定期的な使用を開始。18歳でボーイフレンドに違法な処方オピオイドを紹介され、最初は経口、次に経鼻で使用。19歳でボーイフレンドが関係を解消し、初めてオピオイド離脱症状を経験。これが原因で、ストリップクラブでのダンサーなど、より危険な薬物探索行動に拍車がかかり、20歳で静脈注射によるヘロイン使用を開始。3年間、毎日1〜2gを静脈注射で摂取し、医療または精神科のケアを受けたことはない。重度の体重減少と、2日前に暴行を受けた状況で治療のため来院。軽度のオピオイド離脱症状があり、緩和のために大麻を喫煙中。1日1箱の喫煙者。
治療アプローチ:
この若い女性は、SUDに関連する複数の生命を脅かす問題を抱えています。安定した住居の欠如、注射薬物使用、栄養失調、性的暴行です。治療の第一歩は、住宅に収容された環境で安全を確保し、ヘルスケアへの関与を支援し、物質や危険な仲間へのアクセスを防ぐことです。軽度のオピオイド離脱症状は、大麻の使用では十分に軽減されないでしょう。彼女をケアに引き込み、住居環境から離れさせる原因となるオピオイドへの渇望を軽減するためには、アゴニスト安定化(ブプレノルフィンまたはメサドン維持療法)を薬物補助治療として検討することが推奨されます。ナルメトルトレキソンによる治療は、離脱症状のリスクを軽減するため、最後のオピオイド使用後7〜14日間は適切ではありません。
効果的なケアは包括的でなければならず、うつ病とPTSDの評価、栄養状態、感染症(心内膜炎、HCV、HIV、性感染症)、禁煙の医学的評価が含まれます。女性のピアサポートは、危険な行動パターンを断ち切り、生殖器の健康を最適化するための重要な社会的構造を提供するでしょう。安全な方法で自立した回復を支援するために、職業カウンセリングが必要です。注射によるオピオイド使用障害の場合、最善の診療には、回復志向の行動を奨励するための偶発性管理の要素と、将来の再発とオピオイド過量摂取の場合に備えての経鼻ナロキソン救助の訓練とアクセスが含まれます。
事例2:コカイン使用障害の男性(55歳)
状況:
55歳の離婚した男性、成人した子供が3人。主治医からコカイン使用障害の安定化のために紹介された。再発性の副鼻腔炎および上気道感染症の治療のために医学的に経過観察されており、最終的に経鼻コカイン使用に関連する鼻中隔穿孔が判明した。過去20年間成功し繁栄した配管事業を経営している。最近5年間同性パートナーとの別れを経験し、そのパートナーとは平均して週3日コカインを使用していた。パートナーの死と薬物使用を家族は知らず、個人的なサポートも欠如している。最近、コカインを使用する他の男性との急速な「出会い系サイト」を利用しており、これらの夜の費用を支えるために経済的な負担を感じ始めている。最後のコカイン使用は1週間前で、重度の渇望を訴えている。他の薬物は使用せず、注射薬物を使用したことはなく、飲酒も稀である。
治療アプローチ:
このケースでは、潜在的に危険なオンラインパートナー探索サイトからの即時離脱のカウンセリングと環境の安全評価に加えて、彼の悲嘆と初期の禁断状態において最も差し迫った危害のリスクは自殺念慮に関連するものです。これはいつでも自殺計画や自殺行動に進行する可能性があります。SUDは自殺企図の有意な増加と関連しているため、入院または住宅治療施設への入所が必要であるかどうかの慎重な評価が適切です。
コカインまたは他の精神刺激剤使用障害に対する特定の薬物補助治療は現在ありませんが、初期の精神刺激剤禁断の典型的な症状である不快気分/抑うつに対する積極的な治療が保証されます。ブプロピオンは弱いドーパミン作動性活性を持つため、コカインへの渇望の改善に寄与する可能性があり、最適な選択肢と考えられます。「カミングアウト」と最近の複雑な悲嘆に対処する文化的に感受性のある療法は回復に不可欠であり、自助グループ支援は対処と癒しを促進する社会的サポートを提供するでしょう。家族教育は通常、ケアの不可欠な要素ですが、このケースに関するいくつかの側面は、個人が家族を直接治療計画に統合する前に、回復プロセスをさらに進める必要があるという注意と考慮を示唆しています。
参考文献
- Becker JB, Koob GF. Sex differences in animal models: focus on addiction. Pharmacol Rev. 2016;68:242-263.
- Berridge KC, Robinson TE. Liking, wanting, and the incentive-sensitization theory of addiction. Am Psychol. 2016;71:670-679.
- Bossert JM, Marchant NJ, Calu DJ, Shaham Y. The reinstatement model of drug relapse: recent neurobiological findings, emerging research topics, and translational research. Psychopharmacology (Berl). 2013;229:453-476.
- Bruchas MR, Land BB, Chavkin C. The dynorphin/kappa opioid system as a modulator of stress-induced and pro-addictive behaviors. Brain Res. 2010;1314:44-55.
- Carlezon WA Jr, Thomas MJ. Biological substrates of reward and aversion: a nucleus accumbens activity hypothesis. Neuropharmacology. 2009;56(Suppl 1):122-132.
- Chartoff EH, Carlezon WA Jr. Drug withdrawal conceptualized as a stressor. Behav Pharmacol. 2014;25:473-492.
- Cheron J, de Kerchove d’Exaerde A. Drug addiction: from bench to bedside. Transl Psychiatry. 2021;11:424.
- Dong Y, Taylor JR, Wolf ME, Shaham Y. Circuit and synaptic plasticity mechanisms of drug relapse. J Neurosci. 2017;37:10867-10876.
- Everitt BJ, Robbins TW. Drug addiction: updating actions to habits to compulsions ten years on. Annu Rev Psychol. 2016;67:23-50.
- Haber SN, Knutson B. The reward circuit: linking primate anatomy and human imaging. Neuropsychopharmacology. 2010;35:4-26.
- Heyer MP, Kenny PJ. Corticostriatal microRNAs in addiction. Brain Res. 2015;1628(PtA):2-16. *Jonkman S, Kenny PJ. Molecular, cellular, and structural mechanisms of cocaine addiction: a key role for microRNAs. Neuropsychopharmacology. 2013;38:198-211.
- Kalivas PW. The glutamate homeostasis hypothesis of addiction. Nat Rev Neurosci. 2009;10:561-572.
- Koob GF. Neurobiology of opioid addiction: opponent process, hyperkatifeia, and negative reinforcement. Biol Psychiatry. 2020;87:44-53.
- Koob GF, Volkow ND. Neurobiology of addiction: a neurocircuitry analysis. Lancet Psychiatry. 2016;3:760-773.
- Lüscher C, Malenka RC. Drug-evoked synaptic plasticity in addiction: from molecular changes to circuit remodeling. Neuron. 2011;69:650-663.
- Lüscher C, Robbins TW, Everitt BJ. The transition to compulsion in addiction. Nat Rev Neurosci. 2020;21(5):247-263.
- Moussawi K, Kalivas PW. Group II metabotropic glutamate receptors (mGlu2/3) in drug addiction. Eur J Pharmacol. 2010;639:115-122.
- Muschamp JW, Carlezon WA Jr. Roles of nucleus accumbens CREB and dynorphin in dysregulation of motivation. Cold Spring Harb Perspect Med. 2013;3:a012005.
- Nestler EJ, Lüscher C. The molecular basis of drug addiction: linking epigenetic to synaptic and circuit mechanisms. Neuron. 2019;102:48-59.
- Pickens CL, Airavaara M, Theberge F, Fanous S, Hope BT, Shaham Y. Neurobiology of the incubation of drug craving. Trends Neurosci. 2011;34:411-420. *Potenza MN, Sofuoglu M, Carroll KM, Rounsaville BJ. Neuroscience of behavioral and pharmacological treatments for addictions. Neuron. 2011;69:695-712.
- Prasad AA, McNally GP. The ventral pallidum and relapse in alcohol seeking. Br J Pharmacol. 2020;177:3855-3864.
- Quigley JA, Logsdon MK, Turner CA, Gonzalez IL, Leonardo NB, Becker JB. Sex differences in vulnerability to addiction. Neuropharmacology. 2021;187:108491.
- Robison AJ, Nestler EJ. Transcriptional and epigenetic mechanisms of addiction. Nat Rev Neurosci. 2011;12:623-637.
- Sinha R. The clinical neurobiology of drug craving. Curr Opin Neurobiol. 2013;23:649-654.
- Smith ACW, Scofield MD, Kalivas PW. The tetrapartite synapse: extracellular matrix remodeling contributes to corticoaccumbens plasticity underlying drug addiction. Brain Res. 2015;1628(Pt A):29-39.
- Wise RA, Koob GF. The development and maintenance of drug addiction. Neuropsychopharmacology. 2014;39:254-262.
- Wise RA, Robble MA. Dopamine and addiction. Annu Rev Psychol. 2020;71:79-106.
- Wolf ME. Synaptic mechanisms underlying persistent cocaine craving. Nat Rev Neurosci. 2016;17:351-365.
- Zilverstand A, Huang AS, Alia-Klein N, Goldstein RZ. Neuroimaging impaired response inhibition and salience attribution in human drug addiction: a systematic review. Neuron. 2018;98:886-903.

