うつ病と病時行動は、共通する炎症経路に対するヤヌスの二面性の応答である
Michael Maes, Michael Berk, Lisa Goehler, Cai Song, George Anderson, Piotr Gałecki, Brian Leonard
BMC Medicine 2012, 10:66
抄録
うつ病が病時行動の一形態であるのか、それとも病時行動の結果であるのか——この問いは、臨床的・基礎的翻訳研究において大きな重要性を持つ。
病時行動とは、感染や免疫的外傷によって引き起こされ、炎症性サイトカインによって媒介される行動の複合体である。急性炎症と戦うためにエネルギーを温存することで回復を促進する、適応的な応答である。
病時行動とうつ病には、現象論的に顕著な類似点がある。たとえば行動抑制、食欲不振・体重減少、メランコリー症状(アンヘドニア)、身体・生理的症状(疲労、痛覚過敏、倦怠感)、不安症状、神経認知症状などである。
しかし臨床的うつ病においては、ある移行が起きる。すなわち、免疫炎症経路の感作、脂質・タンパク質・DNAへの酸化ストレス・窒素化ストレスによる進行性の障害、そして自己エピトープに向けられた自己免疫応答への移行である。後者のメカニズムは神経進行性プロセスの基盤となり、複数回の抑うつエピソードが神経組織の損傷と、それに伴う機能的・認知的後遺症を引き起こす。
このように、共通する免疫炎症経路が、病時行動の生理と臨床的うつ病の病態生理の両方を支えており、それが両者の現象論的な部分的重複を説明する。炎症はヤヌスの二面性をもつ応答を引き起こす可能性がある——良い急性の側面(病時行動を通じた保護的炎症の生成)と、悪い慢性の側面(たとえば臨床的うつ病。これはより明確でないトリガーに続く、(神経)炎症と(神経)変性プロセスの間の正のフィードバックループを持つ、生涯にわたる障害である)。
はじめに
臨床的うつ病と病時行動の間に現象論的類似性があること、そして両者が共通する経路——すなわち炎症反応系(IRS)の活性化——を共有する可能性があることを最初に示唆したのは、1993年の報告である。
病時行動とは、多くの哺乳類種において急性感染と組織損傷によって典型的に引き起こされる行動の複合体である。その特徴的な行動パターンは以下からなる:倦怠感、痛覚過敏、発熱、無気力と周囲への無関心、嗜眠、行動抑制、運動活性・探索・毛づくろいの低下、生殖能力の低下、アンヘドニア、傾眠と睡眠傾向の増加、食欲不振・体重減少、集中力の低下、不安。
病時行動はIL-1、TNFα、IL-6などの炎症性サイトカイン(PICs)の影響を通じて媒介されるという証拠が豊富にある。
この文脈において、臨床的うつ病がとりわけPICsおよびC反応性タンパク・ハプトグロビンなどの急性期タンパク質の増加を特徴とする免疫炎症性障害であるという豊富な証拠がある。
大うつ病の特徴的症状には、食欲不振、体重減少、疲労、嗜眠、睡眠障害、痛覚過敏、運動活性の低下、集中力の低下が含まれる。さらに、食欲不振・体重減少・精神運動抑制といった「植物的症状」は、臨床的うつ病における炎症マーカー(上記3つのPICsすべてによって合成が誘導される急性期タンパクであるハプトグロビンの血漿中濃度増加など)と有意に関連している。
こうして、病時行動と臨床的うつ病の両者には、行動的にも炎症的にも著しい類似性があると結論できる。
病時行動の性質
炎症性誘発因子(急性ウイルス・細菌感染や炎症性外傷など)は自然免疫系の受容体などの「センチネル(番兵)」によって検出され、炎症組織内の免疫細胞を標的とするPICsなどの炎症性メディエーターを活性化する。
適応的な炎症応答は、トリガーが排除され、損傷組織が修復されると終息する。これは「炎症の収束」として知られる現象である。
このセクションで説明するように、PICsが誘導する病時行動は、炎症の収束と、炎症中に増大するエネルギー需要において重要な役割を果たす。
病時行動とエネルギー消費
病原体の脅威に対抗することは大量のエネルギーを消費し、利用可能なエネルギーを配給する。TNFαシグナルなどのPICシグナルは、この増大したエネルギー需要とエネルギー供給のバランスを調節し、食物摂取・エネルギー消費・基質利用を制御する。
PICs は負のエネルギーバランス(脂肪分解の亢進、組織タンパク質の喪失と筋タンパク質合成の低下、糖新生)と自発的エネルギー利用の低下を特徴とする、この著しく増大したエネルギー需要において中心的な役割を果たす。
中枢神経系(CNS)は、PICsが求心性迷走神経シグナルを活性化すること、TNFαが孤束核の感覚核に作用すること、および3つのPICSすべてが異なる経路を通じて脳に侵入することを通じて、末梢の炎症応答に関する神経的・体液的シグナルを受け取る。
これらのPICsはその後、運動活性・神経認知・生殖活性などのエネルギーを消費するプロセスをシャットダウンする。こうして代謝エネルギーは脳と一部の末梢臓器から引き上げられ、侵入した病原体の有害な影響に対抗するために再配分される。このプロセスによって節約されたエネルギーは発熱に寄与し、免疫細胞の炎症状態を増強する。
無気力・倦怠感・傾眠・精神運動抑制・認知障害・性欲低下などの病時行動症状の多くは、運動・性的・脳活動を制限し、それによって代謝エネルギーを一次感染との戦いに向けるために機能する。
免疫応答は高度にカロリー依存的であり安静時エネルギー消費を増大させる一方、運動抑制などの病時行動応答はこの重要なエネルギーを温存しうる。
病時行動と発熱
軽度から中等度の発熱(高熱とは対照的に)は正の適応応答であり、宿主の防御と感染への抵抗力を強化する。たとえば多形核白血球の貪食能と運動性を高め、細菌を殺し、ウイルスの複製を抑制する。加えて、IFNsなどのPICsやサイトカインは発熱中により活性化される。
発熱性のIL-1と非発熱性のIL-18の相対的なバランス、および異なるCNS部位におけるそれらの内因性阻害因子が、発熱の有無と程度に寄与しうる。かつては感染と戦うために患者に人工的に発熱を誘発することさえ行われていた。
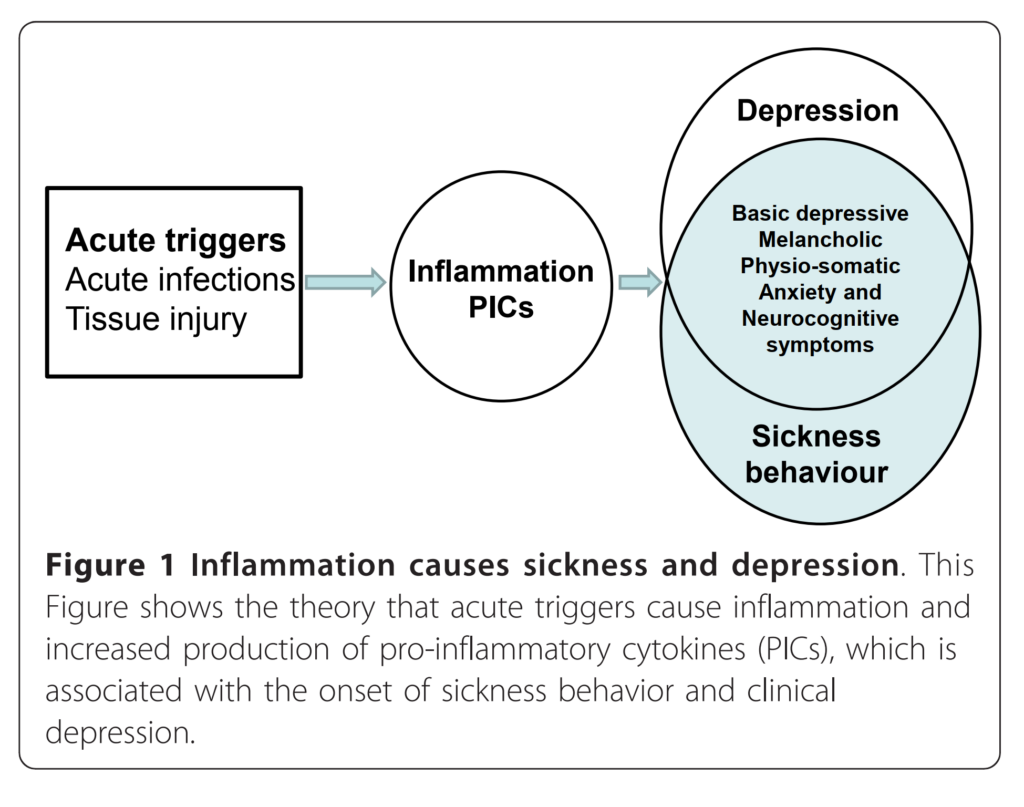
病時行動と食欲不振・体重減少
炎症誘発性の食欲不振は、刺激の大きさに比例し、刺激前の体重とは反比例する。食欲不振は、他の場合には細菌の産生を活性化するであろう鉄の摂取を制限するという仮説がある。しかしこれはきわめて投機的であり、より説得力ある適応機能として、食欲不振によるカロリー制限が炎症と病時行動を軽減するという見方がある。
運動抑制と食欲不振は、除脂肪体重の喪失・タンパク質異化の亢進・体タンパク質と体脂肪の喪失をもたらしうる。これらが合わさって、炎症誘発性の体重減少、最終的には悪液質(カヘキシア)を説明しうる。
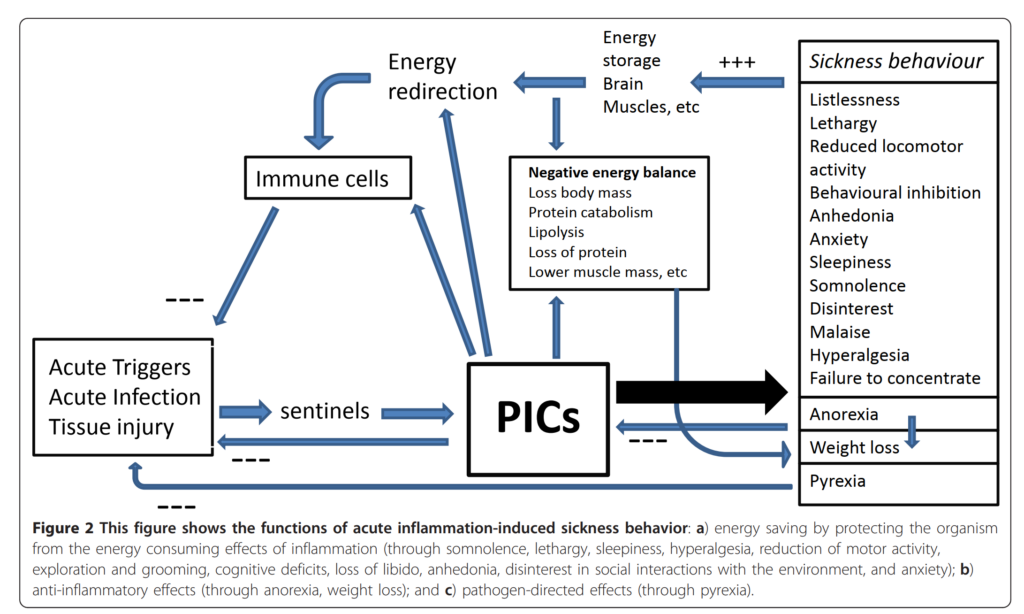
図2の説明:急性炎症誘発性の病時行動の機能を示す。① 傾眠・嗜眠・睡眠傾向・痛覚過敏・運動活性・探索・毛づくろいの低下・認知障害・性欲低下・アンヘドニア・環境への無関心・不安を通じた、炎症のエネルギー消費効果からの生体保護(エネルギー節約)。② 食欲不振・体重減少を通じた抗炎症効果。③ 発熱を通じた病原体指向効果。
うつ病と病時行動の症状的・行動的類似点と相違点
表1の翻訳:
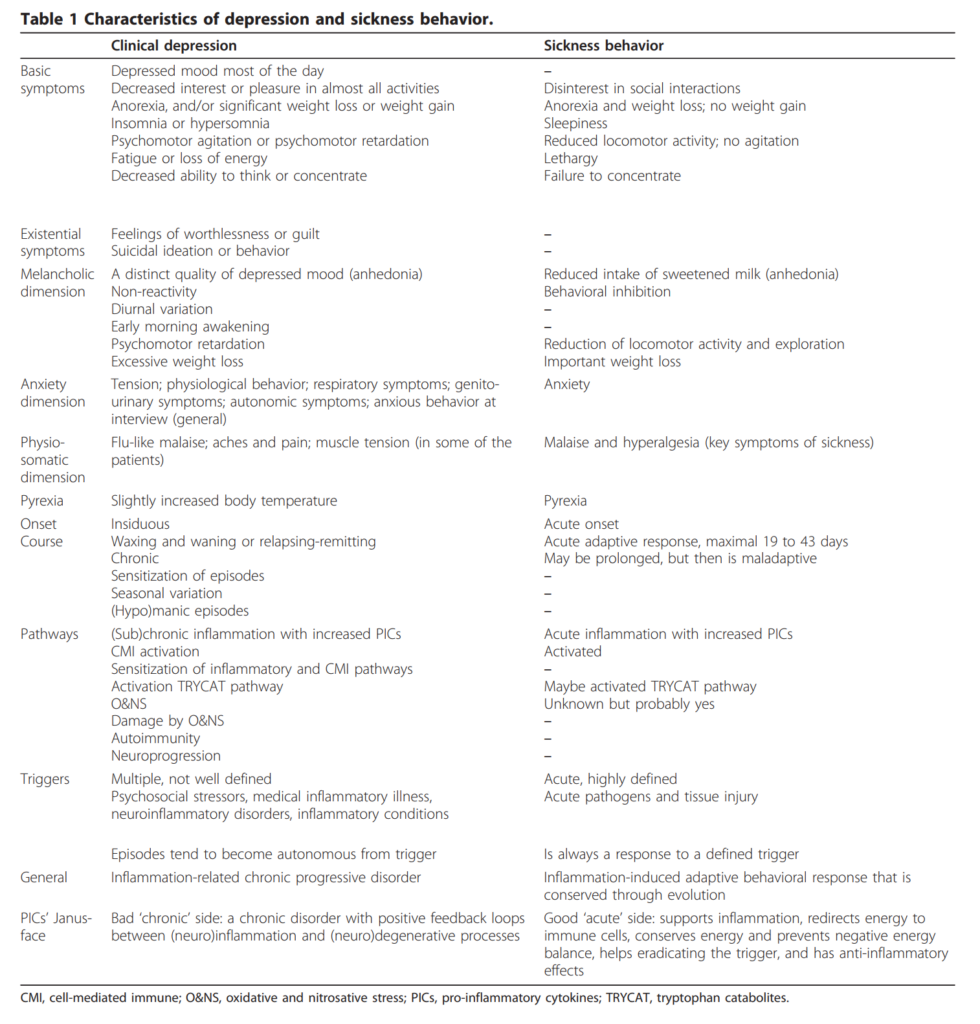
臨床的うつ病 vs 病時行動
「基本症状」について:臨床的うつ病では、ほぼ1日中続くうつ気分、ほぼすべての活動に対する興味・喜びの減退、食欲不振および/または著しい体重減少・増加、不眠または過眠、精神運動焦燥または抑制、疲労またはエネルギー喪失、思考力・集中力の低下がある。病時行動では、周囲との社会的相互作用への無関心、食欲不振・体重減少(体重増加はない)、傾眠、運動活性の低下(焦燥なし)、嗜眠、集中力の低下がある。
「実存的症状」について:臨床的うつ病では、無価値感・罪悪感、自殺念慮または自殺行動がある。病時行動では該当なし。
「メランコリー次元」について:臨床的うつ病では、うつ気分の際立った性質(アンヘドニア)、非反応性、日内変動、早朝覚醒、精神運動抑制、著明な体重減少がある。病時行動では、甘味付き牛乳摂取量の減少(アンヘドニア)、行動抑制があるが、日内変動・早朝覚醒はない、運動活性・探索の低下、著明な体重減少がある。
「不安次元」について:臨床的うつ病では、緊張・生理的行動・呼吸症状・泌尿生殖器症状・自律神経症状・面接時の不安行動がある。病時行動でも不安がある。
「身体・生理的次元」について:臨床的うつ病では、インフルエンザ様倦怠感、疼痛・痛み、一部の患者で筋緊張がある。病時行動では倦怠感・痛覚過敏(病時の中心症状)がある。
「発熱」について:臨床的うつ病ではわずかな体温上昇。病時行動では発熱。
「発症・経過」について:臨床的うつ病は緩徐な発症、増悪・寛解または再発・寛解、慢性、エピソードの感作、季節的変動、(軽)躁病エピソードがありうる。病時行動は急性発症、急性適応応答で最長19〜43日、延長することもあるがその場合は不適応、季節的変動なし、躁病エピソードなし。
「経路」について:臨床的うつ病は亜慢性炎症とPICs増加、細胞性免疫(CMI)活性化、炎症・CMI経路の感作、TRYCATsの活性化、酸化・窒素化ストレス(O&NS)、O&NSによる障害、自己免疫、神経進行。病時行動では急性炎症とPICs増加、CMI活性化あり、感作なし、TRYCAT経路は活性化されている可能性あり、O&NSは不明だがおそらくあり、O&NS障害なし、自己免疫なし、神経進行なし。
「トリガー」について:臨床的うつ病は多因子的・明確でない(心理社会的ストレス、医学的炎症性疾患、神経炎症性障害、炎症状態)。病時行動は急性・明確に定義されたもの(急性病原体・組織損傷)。臨床的うつ病のエピソードはトリガーから自律的になる傾向がある。病時行動は常に明確なトリガーへの応答。
「全体的特徴」について:臨床的うつ病は炎症関連の慢性進行性障害。病時行動は進化を通じて保存された炎症誘発性の適応行動応答。
「PICs のヤヌスの顔」について:臨床的うつ病は悪い「慢性」側面(神経炎症と神経変性プロセスの間の正のフィードバックループを持つ慢性障害)。病時行動は良い「急性」側面(炎症をサポートし、エネルギーを免疫細胞に再配分し、エネルギーを節約して負のエネルギーバランスを防ぎ、トリガーの排除を助け、抗炎症効果を持つ)。
DSM-IV-TRによれば、臨床的うつ病の診断は9つの基本症状のうち少なくとも5つが少なくとも2週間存在する場合に下すことができる。表1はこれらの9症状と、3つの部分的に重複する症状次元——①メランコリー、②不安、③身体・生理的次元——を示している。なお、多変量統計解析(パターン認識法)がこれらの基本症状と3つの症状次元を確認・妥当化しており、これらはバイオマーカーによって外的妥当性が確認されている。
うつ病と病時行動の明らかな相違点は自殺念慮・罪悪感・無価値感であり、うつ病の独自の実存的状態を示す症状である。また、「倦怠感の病態理論(malaise theory of depression)」——倦怠感、すなわち病時行動の中心症状をうつ病の核心的「感情」とみなす理論——も重要である。これによれば、気分の低下とうつ病のより独自の実存的状態は倦怠感の産物であり、病時行動に罹患していながら自分が病気であることを知らない人間が、そのエネルギー欠如と神経認知障害を個人的失敗と解釈してしまい、罪悪感や無価値感が生じると考える。
ただし多変量統計解析は、うつ病患者のうち倦怠感を含む身体・生理的症状に苦しむのは一部であることを示しており、これは「倦怠感がうつ病の核心的感情である」という見解と相容れない。
うつ病のステージングと病時行動の経過の比較
一部の患者は単一のうつ病エピソードのみを経験することがあるが、過去20年間の縦断的研究は、臨床的うつ病が典型的にはエピソード性または生涯にわたる疾患であることを示している。うつ病は古典的に自己限定的で短期間(6〜9ヶ月)の障害とみなされてきたが、その経過は大きく異なりうる。慢性的なエピソード(慢性うつ病)や頻繁な再発(反復性うつ病)をとりうる。さらに、うつ病患者の最大15%が治療抵抗性(少なくとも2回の適切な抗うつ薬試験に対する失敗として定義される)を発症しうる。
また、躁病・軽躁病エピソードを伴う双極性うつ病や、抑うつと躁/軽躁症状が混在する混合状態も存在する。
脳は最も代謝的に活性な組織の一つであり、エネルギーと気分は密接に絡み合っている。うつ病は脳のエネルギー産生の低下と関連し、躁病はエネルギー消費の増加と関連する一方、病時行動はエネルギーを温存する行動応答である。
単極性・双極性うつ病のいずれも進行性疾患の特徴を持つ。軽度または非特異的な症状から始まり、閾値下症状の前駆期に進行し、次いで急性エピソード、再発、または持続的・難治性疾患の慢性形態へと進行する段階を経ることが多い。より早い発症と、エピソードの長さ・数の増加は、さらなる再発への脆弱性増加と不良な転帰と関連する。この進行性経過は機能的悪化と神経認知障害を伴う。
また、感作モデルがエピソード再発のモデルとして提案されている。感作とは、心理的または器質的ストレッサーへの繰り返しの暴露が、これらのストレッサーへの再暴露に対する感受性を時間依存的・進行的に増加させることを意味する。McEwenのアロスタティック負荷モデルもこの進行パターンの記述に適用されている。また、単極性・双極性うつ病と抑うつサブグループ(産後うつ病など)で季節的変動が頻繁にみられ、たとえば春にピークがある。
これに対し、病時行動は急性かつ短期の状態であり、急性感染・外傷に対処して回復を促進するために生物学的に適切である。明らかに、軽躁/躁病症状、時間経過に伴う進行性悪化、季節的変動は病時行動の特徴ではない。
病時行動が延長または不適切に活性化されることがある。このような延長した病時行動複合体は機能不全となりやすい。慢性感染症や(自己)免疫疾患でもこれは起こりうる。運動・活動障害は病時行動に典型的に関連し、急性・慢性疾患(心疾患・関節リウマチ・がんを含む)における疲労・うつ・睡眠障害クラスターの一部をなす。一部の個人ではこれらの症状がICU入院後や放射性物質投与後に数年にわたって持続することもある。この状態はもはや有益でないにもかかわらず「病時行動」と呼ぶべきか、という問いが生じる。
臨床的うつ病と病時行動を支える共通経路
炎症と細胞性免疫
ヒトおよび齧歯類の研究は、PICsが病時行動の中心的メディエーターであることを明確に示している。炎症性トリガーは「神経軸(neuraxes)」すなわち上行性神経経路を誘発し、代謝的・消化器系・心血管系の課題に関する情報を、ストレス関連行動を媒介する脳領域に伝達する。
感染・免疫活性化は、末梢からPICsが媒介するボトムアップの炎症経路を活性化し、延髄尾側の迷走神経背側複合体・腹側延髄に達する。内臓感覚経路を介して脳に伝達されたこれらの炎症的挑戦は、病時行動、うつ病様・不安様行動を駆動する。さらに、PICsは内皮細胞トランスポーターによって脳に能動輸送されるか、血液脳関門欠損部位を通じて拡散しうる。これが全身性炎症が神経炎症とミクログリア活性化を引き起こす理由を説明しうる。
臨床的うつ病では、亜慢性炎症・CMI活性化の証拠があり、IFNγ関連経路の活性化を伴うTh1様応答を特徴とする。最近のメタ解析と最新の論文は、ヒトのうつ病においてPICs(特にIL-6・TNFα・IL-1)の増加とCMI活性化(ネオプテリンと可溶性IL-2受容体〔sIL-2Rs〕の高値で証明される)を確認している。
増加したネオプテリンはIFNγ介在性マクロファージ活性化の増加マーカーである。IFNαベースの免疫療法はC型肝炎ウイルス患者の多くに身体・生理的症状・抑うつ症状を誘発する。このIFNαベース免疫療法中の抑うつ症状の発症は、単球性サイトカイン・Th1様サイトカイン・Th2様サイトカインの上昇を含むサイトカインネットワークの誘導と強く関連している。
PICsとCMIサイトカインの増加は抑うつ症状を産生しうる。臨床的に関連する急性相モデルはサイトカイン投与によって提供される。動物実験では、IL-1・IL-6・TNFαなどのPICsおよびIL-2・IFNγなどのCMIサイトカイン(いずれも約50 μg/kg)が以下を誘発しうることが強く示されている:① 病時行動、② うつ病様症状(意欲行動の喪失・社会的探索の減少・食欲不振・体重減少・自発運動活性の低下・記憶障害など)、③ メランコリー症状(スクロースまたはチョコレートミルク溶液に対する選好の低下で示されるアンヘドニア、視交叉上核への作用を通じた概日時計の変化)、④ 不安(高架式十字迷路での不安原性効果・条件性恐怖記憶の増大)、⑤ 身体・生理的症状(疲労・痛覚過敏・自律神経症状)。
補償的(抗)炎症反射系(CIRS)の存在も重要である。IL-10(負の免疫調節サイトカイン)およびTGFβ(増殖抑制因子)産生の増加などの炎症性反射阻害が調節機構の例である。
臨床的うつ病においても比較可能な対抗調節プロセスが記述されている:IL-1受容体拮抗薬(IL-1RA)の合成増加(IL-1の機能を阻害する)、PICs誘発性のコルチゾール軸活性化とその結果としてのグルココルチコイドの免疫抑制活性、IL-10・IL-1RA・グルココルチコイドの産生を増加させることによる保護的なIL-6産生増加、IL-2への結合によりリンパ球増殖に必要なIL-2の量を制限するIL-2R濃度増加、免疫抑制因子として作用するハプトグロビンなどの急性期タンパク質の産生増加、リンパ増殖応答を抑制しうるプロスタグランジン産生増加、血漿トリプトファン濃度の低下(次節参照)。
著者らはこの補償的反射系を「補償的(抗)炎症反射系(CIRS)」と命名することを提案する。
病時行動は保護的炎症応答をサポートし(トリガーの排除を助け、エネルギーを炎症細胞に再配分する)、炎症の有害な影響から保護し(負のエネルギーバランスなど)、同時に抗炎症反射として機能する(カロリー制限と体重減少の抗炎症効果)。したがって、病時行動そのものが急性炎症に対するCIRS応答とみなされるべきである。
TRYCATsとトリプトファン経路
炎症と関連して一部のうつ病患者に確立された新しい経路として、トリプトファン代謝産物(TRYCAT)経路の活性化がある。この経路の最初の律速酵素はインドールアミン2,3-ジオキシゲナーゼ(IDO)である。IDOはIFNγとIL-1・TNFαなどのPICsによって活性化され、トリプトファンの異化を誘導し、トリプトファン枯渇と、キヌレニン・キヌレン酸・キサンツレン酸・キノリン酸などのTRYCATsの合成増加をもたらす。
うつ病では血漿トリプトファンの低下が頻繁にみられ、炎症バイオマーカー(急性期反応物質・サイトカイン増加)とCMI活性化(血清ネオプテリン・sIL-2Rs増加)のバイオマーカーと強く関連している。
動物実験ではIDO活性化が病時行動とうつ病様行動を分離しうることが最近示されている。BCG(ウシ型弱毒結核菌)接種はIDO活性化とPICs・CMIサイトカインの上昇を引き起こし、急性の病時行動エピソードの後にBCG投与1週間後から始まる慢性的なうつ病様症状を誘発した。病時行動はWT(野生型)マウスとIFNγR(−/−)マウスの両方で同等に誘発されたが、ミクログリアでのIDO活性化とその後のうつ病様行動にはIFNγとTNFαの両方が必要であった。またIDO欠損マウスはBCGのうつ病誘発効果に対して抵抗性を示したが、BCG投与後の正常な炎症応答は示した。
ただしこれらのTRYCATデータを臨床的うつ病に外挿することは難しく、臨床的結果は矛盾している。一連の研究では、うつ病患者へのトリプトファン負荷後に尿中TRYCATsの変化は認められなかった。しかし別の研究では抑うつ状態においてキヌレン酸レベルの低下とキヌレニン/キヌレン酸比の増加が観察された。この比率はキヌレニンとその一部の代謝産物(キノリン酸など)が抑うつ原性・不安原性・興奮毒性・神経毒性を持つ一方、キヌレン酸は神経保護的であることから、うつ病の病態生理にとって重要でありうる。
要約すると、急性炎症状態(IFNα免疫療法中など)ではIDO活性化はうつ病様行動の発症と強く関連しているが、臨床的うつ病ではそうではない。身体・生理的症状または自殺行動を持つ一部の患者のみが相対的なTRYCAT増加を示す。
IDO活性化は保護的CIRS機能を持つ。IDO誘発性の血漿トリプトファン低下とTRYCAT産生増加は、T細胞の活性化・増殖を減弱させることで一次免疫炎症応答を減弱させうる。この反射阻害はうつ病の自然寛解に関与している可能性があり、うつ病が時に自己限定的障害であるという観察と一致する。
うつ病を病時行動と区別する有害な免疫炎症経路
感作と自己免疫への移行
反復するうつ病エピソードによって免疫炎症応答が感作されるという証拠がある。CMI活性化のバイオマーカーであるネオプテリンは、1回のみエピソードを経験した患者より2回以上経験した患者で有意に増加している。同様に、血漿IL-1とTNFαは3回以上のエピソードを経験したうつ病患者で有意に増加している。
さらに、炎症誘発性のIL-1と関連したCMI刺激の投与がサイトカインネットワークの誘導を通じてうつ病誘発性サイトカインの病原性応答を増幅させ、炎症誘発性行動応答を増強しうる可能性が示唆されている。エピソード数の増加が再発リスクと治療抵抗性を増大させることが知られていることから、これらの所見は免疫炎症経路の感作が新たなうつ病エピソード発症への脆弱性を増大させることを示唆している。
免疫炎症メカニズムは、臨床的うつ病における5-HT抗体活性の高率(54.1%)、メランコリアにおける高率(82.9%)が正常対照(5.7%)と比較して高いことも説明しうる。この5-HTに対する自己免疫活性は、炎症バイオマーカー(IL-1・TNFα増加)とCMI活性化(ネオプテリン増加)のバイオマーカーと有意に関連している。
また、5-HTに対する自己免疫活性は過去のうつ病エピソード数とも関連しており、過去のうつ病エピソードへの暴露が抗5-HT抗体活性を増加させ、それが新たなうつ病エピソード発症リスクを高める可能性があることを示唆している。
O&NS障害への移行
多くの炎症性状態と同様に、臨床的うつ病は酸化・窒素化ストレス(O&NS)経路の活性化を伴う。O&NSは、うつ病におけるCoQ10・亜鉛・グルタチオンなどの抗酸化物質レベルの低下と免疫炎症応答によって増幅されており、抗酸化物質の低下・炎症・O&NS経路の活性化の間の悪循環を持続させる。
うつ病は活性酸素・窒素種(ROS/RNS)の増加だけでなく、脂質・タンパク質・DNA・ミトコンドリアへのO&NS障害をも特徴とする。これらのプロセスにおいてO&NS経路は膜脂肪酸と機能タンパク質の化学的構造を変化させうる。これら変化した脂肪酸とタンパク質が免疫原性を帯びるとき、これらの「ネオエピトープ」に向けられた自己免疫応答が生じ、エピトープの機能や化学的構造をさらに障害しうる。
神経進行への移行
臨床的うつ病において有害な影響を及ぼし、病時行動とは無関係な別の免疫炎症関連経路が「神経進行(neuroprogression)」である。これは神経変性・神経新生の低下・神経可塑性・アポトーシスの段階依存的でかつ潜在的に進行性のプロセスである。
多くの(すべてではないが)うつ病患者は進行性疾患の特徴を示す。より長い罹患期間とより頻繁なうつ病エピソードを持つ人は、その後の再発リスクが高い。再発エピソードはより多くの認知障害と関連する——記憶パフォーマンスはうつ病エピソードごとに2〜3%低下する。うつ病エピソードは認知症リスクの増加とも関連する。またより多くのうつ病エピソードは基礎的な脳変化、たとえば眼窩前頭皮質・前帯状皮質・海馬・基底核の体積減少と関連している。メタ解析では慢性うつ病(2年超)または反復性うつ病患者において海馬体積が有意に減少し、これがエピソード数と関連することが示された。治療抵抗性と罹患期間は右尾状核・左被殻体積の減少と関連する。
うつ病と病時行動の病因論的因子
病因論的に、病時行動は急性感染・炎症性外傷に対する急性期の適応CIRS行動として概念化される。しかし収束相が誘発されない場合——たとえばIRSが病原体を排除できなかった場合——炎症はCIRSにもかかわらず持続し、慢性炎症状態を引き起こしうる。
病時行動がこの急性から慢性への移行を防ぐ上で重要な役割を果たすのは、負のエネルギーバランスを補償し、活性化された免疫細胞にエネルギーを再配分すること等による。エネルギー貯蔵が枯渇するまでの移行時点は、エネルギー貯蔵の性質に応じて19〜43日と推定されている。
一方、臨床的うつ病には慢性的な炎症プロセスが伴い、以下のような多様なトリガー因子と関連する:心理社会的ストレス、脳卒中・アルツハイマー病・ハンチントン病・パーキンソン病・多発性硬化症などの脳疾患、心血管疾患、COPD、関節リウマチ・SLE・炎症性腸疾患、糖尿病・代謝症候群、HIV感染、がん、細菌トランスロケーション、産後期、血液透析、IFNα免疫療法。
うつ病においては病原体は主要な役割を果たさない。急性感染やEBV感染がうつ病発症のトリガーとなるという十分な質のエビデンスはないが、HIV感染や腸内グラム陰性菌のトランスロケーション増加などの慢性感染は臨床的うつ病と頻繁に関連する。
重要な点として、うつ病患者でより多くの再発エピソードを経験するにつれて、ストレスフルなトリガーがうつ病の発現に必要なくなっていく。9回以上の過去エピソードの後、トリガーとうつ病の関連は弱まり、エピソードはトリガーから切り離されて自律的に出現する。これもうつ病が進行性障害であり、エピソードが感作されるという知見によって説明されうる。
延長した・誇張した・不適応な病時行動はうつ病か
延長・誇張・不適応な病時行動という新しい概念を記述した文献がある。翻訳モデルでは、誇張した炎症・神経免疫応答は、いわゆる「延長した」病時行動——記憶障害を含む——と関連している。こうした誇張した応答は老齢マウスで観察される。
しかしうつ病は延長した「病時行動」の結果として生じる不適応症候群ではなく、慢性的な基礎免疫炎症・変性プロセスの帰結であると考えられる。この状態は適応応答ではもはやないにもかかわらず「延長した」病時行動と呼ぶことはできない——後者の用語は炎症性外傷に対する短期的適応応答を意味するからである。
うつ病を病時行動の進化的産物として感染からの保護と関連づける新仮説もある。しかしこれらの仮説は、臨床的うつ病が単純な行動応答ではなく、進行性の神経生物学によって駆動されるカスケードが進行性経過と病態生理につながる進行性障害であることを考慮に入れていない。
抗うつ薬治療
抗うつ薬は正常ボランティアと動物モデルにおいて有意な免疫調節・免疫抑制効果を持つ。三環系抗うつ薬(TCAs)と選択的セロトニン再取り込み阻害薬(SSRIs)はIL-1β・TNFα・IL-6などのPICs産生を減弱させる。ほとんどの抗うつ薬(TCAs・SSRIs・可逆的モノアミンオキシダーゼA阻害薬・セロトニン・ノルアドレナリン再取り込み阻害薬・非定型抗うつ薬〔チアネプチンなど〕)はすべてIL-10(負の免疫調節サイトカイン)の産生を増加させ、かつ/またはIFNγの産生を低下させ、IFNγ/IL-10比の低下をもたらす。
しかしうつ病患者における生体内での効果はより不明確である。抗うつ薬のサブクロニック治療はうつ病患者の炎症徴候を一貫して減弱させるわけではない。最近のメタ解析では、SSRIs以外の抗うつ薬サブクラスは炎症性サイトカイン濃度を減弱させなかった。
臨床的うつ病では、抗うつ薬の免疫抑制効果に対する「抵抗性」が伴うようである。これは、免疫炎症経路が抗うつ薬によってはブロックできないプロセスによって継続的に活性化されていることを示唆しうる——たとえばネオ抗原決定基に向けられた自己免疫応答やグラム陰性菌の細菌トランスロケーション増加によって。
抗うつ薬は炎症治療において確立された免疫調節効果を持つにもかかわらず、臨床的うつ病における寛解は免疫炎症経路の正常化と関連しない。増大した活性と免疫炎症経路・O&NS経路・自己免疫応答・神経進行の感作が、うつ病のステージング——たとえば治療抵抗性と再発——を部分的に決定する。
したがって、うつ病において炎症・Th1活性化・O&NS・低下した抗酸化物質レベル・神経進行を標的とする新たな併用治療戦略が開発されている。たとえばスタチン・アセチルサリチル酸・ミノサイクリン・亜鉛・N-アセチルシステイン・クルクミン・ω3多価不飽和脂肪酸などである。
結論
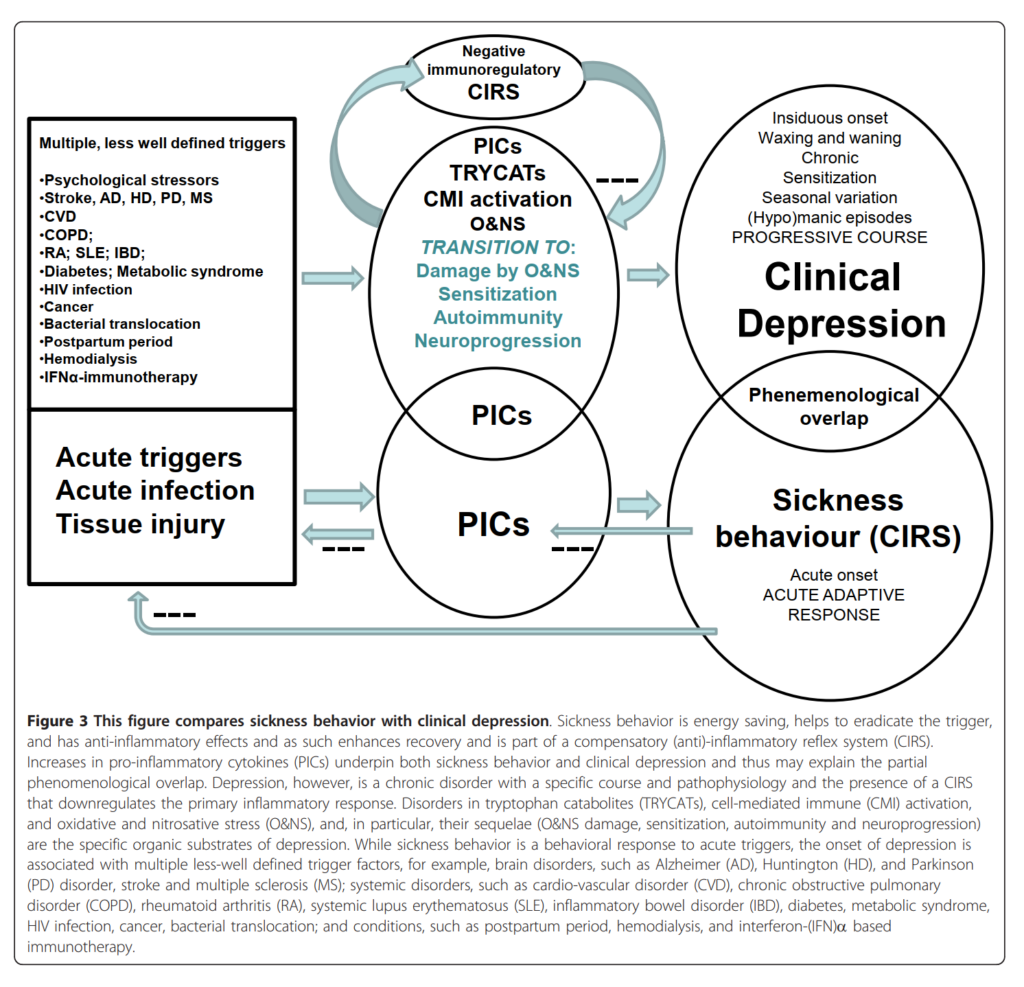
図3の説明:病時行動と臨床的うつ病を比較する。病時行動はエネルギーを節約し、トリガーの排除を助け、抗炎症効果を持ち、回復を促進するCIRS(補償的〔抗〕炎症反射系)の一部である。PICs(炎症性サイトカイン)の増加が病時行動と臨床的うつ病の両方を支え、部分的な現象論的重複を説明する。うつ病は特定の経過と病態生理を持つ慢性障害であり、一次炎症応答を調節するCIRSを伴う。TRYCATs(トリプトファン代謝産物)異常、CMI(細胞性免疫)活性化、O&NS(酸化・窒素化ストレス)、特にその後遺症(O&NS障害・感作・自己免疫・神経進行)がうつ病の特異的な器質的基盤である。病時行動は急性トリガーへの行動応答であるのに対し、うつ病の発症は多様なトリガー因子と関連する。
病時行動は回復を促進するCIRS応答であり、エネルギーを節約し、トリガーの排除を助け、抗炎症効果を持つ。病時行動とうつ病の基本症状・メランコリー・身体生理的・不安症状次元は、横断的に現象論的類似性を持つ。しかし重要な相違として、病時行動の中心症状である倦怠感はうつ病患者の一部にしかみられず、有意な発熱は病時行動にのみ限られる。さらに、うつ病は食欲不振・体重減少ではなく過食・体重増加を伴うことも多い。
翻訳的研究は、炎症経路が病時行動と臨床的うつ病の両方の原因となりうることを示しており、両者の部分的な現象論的重複を説明しうる。
臨床的うつ病は、一次免疫炎症応答を調節するCIRS、および炎症とROS/RNS過剰産生からCMI応答の感作・進行性O&NS障害・自己免疫応答への移行を伴う。後者の経路は神経進行性プロセスの基盤であり、複数のうつ病エピソードが神経組織の損傷とその機能的・認知的後遺症を引き起こす。
病時行動も免疫炎症経路によって誘導されるが、臨床的うつ病とは対照的に、病時行動複合体は一次トリガーからの回復を促進する有益なCIRS効果を持つ。急性炎症が19〜43日以内に収束しない場合、慢性炎症が続き、慢性炎症病理への移行を引き起こしうる。病時行動はこの移行を防ぐ上で重要な役割を果たす。
急性感染は典型的に病時行動を引き起こすが、急性病原体が臨床的うつ病に主要な役割を果たすという証拠は少ない。トラウマ的な生活上の出来事は炎症状態を誘発し臨床的うつ病に至りうるが、心理社会的ストレスと病時行動の関連は記述されていない。
以上のことから、病時行動が有益なCIRS応答であるのに対し、臨床的うつ病は障害をもたらす進行性の障害である。炎症はこのようにしてヤヌスの二面性をもつ応答を引き起こす——良い「急性」保護的炎症側面(CIRSとしての病時行動を含む)と、悪い「慢性」側面(明確でないトリガーに続く〔神経〕炎症と〔神経〕変性プロセスの間の正のフィードバックループを持つ慢性障害である臨床的うつ病)。このヤヌスの顔はまた、進化を通じて保存された炎症誘発性の適応行動応答から、産業化社会で有病率が増大している炎症関連慢性進行性障害への移行をも表している。
参照文献リストを翻訳します。著者名・雑誌名・巻号頁はそのまま残し、論文タイトルのみ日本語に訳します。
参照文献リスト
- Maes M: 大うつ病における急性期反応のレビュー。Rev Neurosci 1993, 4:407-416.
- Maes M, Meltzer HY, Scharpe S, Cooreman W, Uyttenbroeck W, Suy E, Vandervorst C, Calabrese J, Raus J, Cosyns P: 大うつ病における精神運動抑制・食欲不振・体重減少・睡眠障害・エネルギー喪失——高ハプトグロビン血症の精神病理学的相関。Psychiatry Res 1993, 47:229-241.
- Holmes JE, Miller NE: 白色ラットの水分摂取・食物摂取・体温に対する細菌性内毒素の影響。J Exp Med 1963, 118:649-658.
- Hart BL: 病気動物の行動の生物学的基盤。Neurosci Biobehav Rev 1988, 12:123-137.
- Maier SF, Wiertelak EP, Martin D, Watkins LR: インターロイキン-1は塩化リチウムと内毒素によって産生される行動性痛覚過敏を媒介する。Brain Res 1993, 623:321-324.
- Yirmiya R: 内毒素はラットにうつ病様エピソードを産生する。Brain Res 1996, 711:163-174.
- Johnson RW: 病時行動の概念——4つの重要な発見の簡潔な年代記。Vet Immunol Immunopathol 2002, 87:443-450.
- Qin L, Wu X, Block ML, Liu Y, Breese GR, Hong JS, Knapp DJ, Crews FT: 全身性LPSは慢性神経炎症と進行性神経変性を引き起こす。Glia 2007, 55:453-462.
- Dantzer R, O’Connor JC, Freund GG, Johnson RW, Kelley KW: 炎症から病時行動とうつ病へ——免疫系が脳を支配するとき。Nat Rev Neurosci 2008, 9:46-56.
- Burton MD, Sparkman NL, Johnson RW: 脳内インターロイキン-6トランスシグナリングの阻害はLPS誘発性病時行動からの回復を促進する。J Neuroinflammation 2011, 8:54.
- Maes M: 大うつ病における免疫応答の証拠——レビューと仮説。Prog Neuropsychopharmacol Biol Psychiatry 1995, 19:11-38.
- Maes M, Bosmans E, Suy E, Vandervorst C, DeJonckheere C, Raus J: うつ病に関連したマイトゲン誘発性リンパ球応答とインターロイキン-1βおよび可溶性インターロイキン-2受容体産生の障害。Acta Psychiatr Scand 1991, 84:379-386.
- Maes M, Scharpe S, Bosmans E, Vandewoude M, Suy E, Uyttenbroeck W, Cooreman W, Vandervorst C, Raus J: メランコリア中の急性期血漿タンパク質の異常——その疾患における炎症プロセス存在のさらなる証拠。Prog Neuropsychopharmacol Biol Psychiatry 1992, 16:501-515.
- Song C, Dinan T, Leonard BE: うつ病患者と正常対照における免疫グロブリン・補体・急性期タンパク質レベルの変化。J Affect Disord 1994, 30:283-288.
- Leonard B, Maes M: 細胞性免疫活性化・炎症・酸化および窒素化ストレス経路とその後遺症・随伴症状が単極性うつ病の病態生理においていかなる役割を果たすかについての機序的説明。Neurosci Biobehav Rev 2012, 36:764-785.
- Berk M, Brnabic A, Dodd S, Kelin K, Tohen M, Malhi GS, Berk L, Conus P, McGorry PD: 疾患のステージは双極性障害の治療反応に影響を与えるか——実証的治療データとステージングモデルおよび早期介入への示唆。Bipolar Disord 2011, 13:87-98.
- Berk M, Kapczinski F, Andreazza AC, Dean OM, Giorlando F, Maes M, Yücel M, Gama CS, Dodd S, Dean B, Magalhaes PV, Amminger P, McGorry P, Malhi GS: 双極性障害における神経進行の基盤となる経路——炎症・酸化ストレス・神経栄養因子への焦点。Neurosci Biobehav Rev 2011, 35:804-817.
- Maes M, Mihaylova I, Kubera M, Ringel K: うつ病における細胞性免疫の活性化——炎症・メランコリア・臨床ステージング・うつ病の疲労と身体症状クラスターとの関連。Prog Neuropsychopharmacol Biol Psychiatry 2012, 36:169-175.
- Dowlati Y, Herrmann N, Swardfager W, Liu H, Sham L, Reim EK, Lanctôt KL: 大うつ病におけるサイトカインのメタ解析。Biol Psychiatry 2010, 67:446-457.
- Liu Y, Ho RC, Mak A: インターロイキン(IL)-6・腫瘍壊死因子α(TNFα)・可溶性インターロイキン-2受容体(sIL-2R)は大うつ病性障害患者において上昇している——メタ解析とメタ回帰。J Affect Disord 2012, 139:230-239.
- Medzhitov R: 炎症2010——古い炎の新たな冒険。Cell 2010, 140:771-776.
- Peters A: 炎症のエネルギー需要。Endocrinology 2006, 147:4550-4552.
- Steinberg GR, Watt MJ, Febbraio MA: AMPKシグナリングのサイトカイン調節。Front Biosci 2009, 14:1902-1916.
- Roubenoff R, Roubenoff RA, Cannon JG, Kehayias JJ, Zhuang H, Dawson-Hughes B, Dinarello CA, Rosenberg IH: リウマチ性悪液質——慢性炎症における除脂肪体重の減少を伴うサイトカイン駆動性の代謝亢進。J Clin Invest 1994, 93:2379-2386.
- Maes M, Kubera M, Obuchowiczwa E, Goehler L, Brzeszcz J: (神経)炎症性・酸化および窒素化ストレス経路によって説明されるうつ病の多発性合併症。Neuro Endocrinol Lett 2011, 32:7-24.
- Charlton BG: うつ病の倦怠感理論——大うつ病性障害は病時行動であり、抗うつ薬は鎮痛剤である。Med Hypotheses 2000, 54:126-130.
- Cunningham-Rundles S, McNeeley DF, Moon A: 免疫応答の栄養素調節のメカニズム。J Allergy Clin Immunol 2005, 115:1119-1128.
- Kluger MJ: 発熱。Pediatrics 1980, 66:720-724.
- Schaffner A: 発熱——治療すべき有用または有害な症状か? Ther Umsch 2006, 63:185-188.
- Rantala S, Vuopio-Varkila J, Vuento R, Huhtala H, Syrjänen J: β溶血性連鎖球菌菌血症における死亡率の予測因子——集団ベーススタディ。J Infect 2009, 58:266-272.
- El-Radhi AS: 過去と現在における発熱の役割。Med J Islamic World Acad Sci 2011, 19:9-14.
- Harden LM, du Plessis I, Roth J, Loram LC, Poole S, Laburn HP: LPS誘発性発熱と病時行動を媒介するにあたっての末梢性IL-6・脳内IL-1β・プロスタノイドの相対的関与の差異。Psychoneuroendocrinology 2011, 36:608-622.
- Lennie TA: 炎症誘発性の食欲不振と体重減少に対する身体エネルギー状態の関係。Physiol Behav 1998, 64:475-481.
- Kluger MJ, Rothenburg BA: 発熱と鉄の減少——細菌感染に対する宿主防御応答としての相互作用。Science 1979, 203:374-376.
- Jung KJ, Lee EK, Kim JY, Zou Y, Sung B, Heo HS, Kim MK, Lee J, Kim ND, Yu BP, Chung HY: 老齢ラット腎臓における炎症性NF-κBおよびAP-1に対する短期カロリー制限の効果。Inflamm Res 2009, 58:143-150.
- MacDonald L, Radler M, Paolini AG, Kent S: カロリー制限はLPS誘発性病時行動を減弱させ、視床下部シグナリング経路を抗炎症バイアスへとシフトする。Am J Physiol Regul Integr Comp Physiol 2011, 301:R172-184.
- Bosutti A, Malaponte G, Zanetti M, Castellino P, Heer M, Guarnieri G, Biolo G: カロリー制限は不活動誘発性の炎症マーカーC反応性タンパク質とペントラキシン-3の変化を調節する。J Clin Endocrinol Metab 2008, 93:3226-3229.
- Kopp HP, Kopp CW, Festa A, Krzyzanowska K, Kriwanek S, Minar E, Roka R, Schernthaner G: 高度肥満患者における炎症性タンパク質に対する体重減少の影響とインスリン抵抗性症候群との関連。Arterioscler Thromb Vasc Biol 2003, 23:1042-1047.
- Jellema A, Plat J, Mensink RP: 肥満男性における空腹時および食後の炎症マーカーとPAI-1抗原の濃度低下は適度な魚油摂取ではなく体重減少によってもたらされる。Eur J Clin Invest 2004, 34:766-773.
- Sharman MJ, Volek JS: 体重減少は過体重男性において超低炭水化物食と低脂肪食後の炎症バイオマーカーの低下をもたらす。Clin Sci (Lond) 2004, 107:365-369.
- Yang WS, Lee WJ, Funahashi T, Tanaka S, Matsuzawa Y, Chao CL, Chen CL, Tai TY, Chuang LM: 体重減少は脂肪組織由来の抗炎症タンパク質であるアディポネクチンの血漿レベルを増加させる。J Clin Endocrinol Metab 2002, 86:3815-3819.
- Maes M, Maes L, Schotte C, Vandewoude M, Martin M, D’Hondt P, Blockx P, Scharpé S, Cosyns P: 単極性うつ病の臨床サブタイプ 第III部——クラスター解析で生成された非活性型と活性型うつ病クラス間の様々な生物学的マーカーにおける量的差異。Psychiatry Res 1990, 34:59-75.
- Maes M, Meltzer HY, Cosyns P, Schotte C: 不安特徴を伴う大うつ病と伴わない大うつ病の存在の証拠。Psychopathology 1994, 27:1-13.
- Maes M: インフルエンザ様倦怠感・疼痛・痛み・疲労などの「機能的」または「心身的」症状は大うつ病、特にメランコリー型うつ病の主要な特徴である。Neuro Endocrinol Lett 2009, 30:564-573.
- Rausch JL, Johnson ME, Corley KM, Hobby HM, Shendarkar N, Fei Y, Ganapathy V, Leibach FH: うつ病患者は高い体温を持つ——5-HTトランスポーター長プロモーター領域の効果。Neuropsychobiology 2003, 47:120-127.
- Szuba MP, Guze BH, Baxter LR Jr: 電気けいれん療法はうつ病患者において概日振幅を増加させ深部体温を低下させる。Biol Psychiatry 1997, 42:1130-1137.
- Boland RJ, Keller MB: うつ病の経過。Neuropsychopharmacology, the 5th Generation of Progress 所収、Davis KL, Charney D, Coyle JT, Nemeroff C 編。New York: American College of Neuropsychopharmacology; 2002:1009-1015.
- Berk M, Conus P, Lucas N, Hallam K, Malhi GS, Dodd S, Yatham LN, Yung A, McGorry P: ステージを設定する——双極性障害における前駆期から治療抵抗性まで。Bipolar Disord 2007, 9:671-678.
- Berk M, Hallam KT, McGorry PD: 経過特定子としてのステージングモデルの潜在的有用性——双極性障害の視点から。J Affect Disord 2007, 100:279-281.
- Berlim MT, Turecki G: 治療抵抗性/難治性大うつ病(TRD)の意味とは何か——現在の無作為化試験の系統的レビュー。Eur Neuropsychopharmacol 2007, 17:696-707.
- Caliyurt O, Altiay G: 躁病エピソードにおける安静時エネルギー消費。Bipolar Disord 2009, 11:102-106.
- Moylan S, Maes M, Wray NR, Berk M: 大うつ病性障害の神経進行的性質——疾患進行と抵抗性への経路、および治療的示唆。Mol Psychiatry(出版予定)。
- Kessing LV: うつ病性障害の経過中におけるうつ病エピソードの重症度。Brit J Psychiatry 2008, 192:290-293.
- Kessing LV, Andersen PK: うつ病性障害患者と双極性障害患者において認知症発症リスクはエピソード数とともに増加するか。J Neurol Neurosurg Psychiatry 2004, 75:1662-1666.
- Post RM, Rubinow DR, Ballenger JC: 感情疾患の縦断的経過における条件付けと感作。Br J Psychiatry 1986, 149:191-201.
- Antelman SM, Levine J, Gershon S: 時間依存性感作——実験室から臨床の扉へ向かう科学的異端説の変遷。Mol Psychiatry 2000, 5:350-356.
- Bell IR, Hardin EE, Baldwin CM, Schwartz GE: 化学物質と騒音への感受性を持つ若年成人における辺縁系症状の増加と感作可能性。Environ Res 1995, 70:84-97.
- Kapczinski F, Vieta E, Andreazza AC, Frey BN, Gomes FA, Tramontina J, Kauer-Sant’anna M, Grassi-Oliveira R, Post RM: 双極性障害におけるアロスタティック負荷——病態生理と治療への示唆。Neurosci Biobehav Rev 2008, 32:675-692.
- Sato T, Bottlender R, Sievers M, Möller HJ: 抑うつエピソードの明確な季節性は混合状態を伴ううつ病患者と伴わない単極性うつ病患者を区別する。J Affect Disord 2006, 90:1-5.
- Sylvén SM, Papadopoulos FC, Olovsson M, Ekselius L, Poromaa IS, Skalkidou A: 産後うつ病の季節性パターン。Am J Obstet Gynecol 2011, 204:413.e1-6.
- Maes M, Cosyns P, Meltzer HY, De Meyer F, Peeters D: 暴力的自殺における季節性——非暴力的自殺または殺人においては季節性なし。Am J Psychiatry 1993, 150:1380-1385.
- Stone EA, Lehmann ML, Lin Y, Quartermain D: 免疫刺激によるマウスのうつ病様行動は、正の動機付け行動に関与する脳領域の神経活性低下を伴う。Biol Psychiatry 2006, 60:803-811.
- Gaykema RPA, Park S-M, McKibbin CR, Goehler LE: LPSは行動と同時に結節乳頭体ヒスタミン作動性システムの活性化を抑制する——免疫感覚経路の新たな標的。Neuroscience 2008, 152:273-287.
- Bower JE, Ganz PA, Aziz N, Fahey JL: 乳がんサバイバーにおける疲労と炎症性サイトカイン活性。Psychosom Med 2002, 64:604-611.
- Kubera M, Obuchowicz E, Goehler L, Brzeszcz J, Maes M: 動物モデルにおいて、心理社会的ストレス誘発性(神経)炎症・アポトーシス・神経新生の低下はうつ病発症と関連する。Prog Neuropsychopharmacol Biol Psychiatry 2011, 35:744-759.
- Leonard BE, Song C: うつ病の齧歯類モデルにおける免疫系の変化。Int J Neuropsychopharmacol 2002, 5:345-356.
- Song C, Leonard BE: うつ病モデルとしての嗅球摘出ラット。Neurosci Biobehav Rev 2005, 29:627-647.
- Gaykema RPA, Goehler LE: LPS刺激による視床下部オレキシンニューロンにおけるFos抑制——病時行動における潜在的役割。Brain Behav Immun 2009, 23:926-930.
- Gaykema RPA, Goehler LE: 上行性尾側延髄カテコールアミン経路は病時誘発性の探索行動障害を駆動する——疲労の脳基盤? Brain Behav Immun 2011, 25:443-460.
- Anisman H, Merali Z: サイトカイン暴露のアンヘドニア原性・不安原性効果。Adv Exp Med Biol 1999, 461:199-233.
- Lyte M, Li W, Opitz N, Gaykema RP, Goehler LE: マウス結腸過形成の病原体感染初期段階における不安様行動の誘発。Physiol Behav 2006, 89:350-357.
- Goehler LE, Lyte M, Gaykema RP: 感染誘発性の内臓感覚シグナルが不安を増強する——精神神経免疫学への示唆。Brain Behav Immun 2007, 21:721-726.
- Castex N, Fioramonti J, Fargeas MJ, Bueno L: 腸管アナフィラキシー後の特定のラット脳核におけるc-fos発現——5-HT3受容体と迷走神経求心性線維の関与。Brain Res 1995, 688:149-160.
- Rossi-George A, Urbach D, Colas D, Goldfarb Y, Kusnecov AW: T細胞スーパー抗原であるブドウ球菌エンテロトキシンAに対する神経・内分泌・食欲不振応答——TNFαへの依存性。J Neurosci 2005, 25:5314-5322.
- Goehler LE, Gaykema RP, Opitz N, Reddaway R, Badr N, Lyte M: 迷走神経求心性線維と中枢自律神経経路の活性化——カンピロバクター・ジェジュニ腸管感染に対する早期応答。Brain Behav Immun 2005, 19:334-344.
- Grossberg AJ, Zhu X, Leinninger GM, Levasseur PR, Braun TP, Myers MG Jr, Marks DL: 炎症誘発性の嗜眠はオレキシンニューロン活性の抑制によって媒介される。J Neurosci 2011, 31:11376-11386.
- Maes M, Bosmans E, Suy E, Vandervorst C, De Jonckheere C, Raus J: 大うつ病における免疫障害——インターロイキン-2受容体の発現亢進。Neuropsychobiology 1990, 24:115-120.
- Maes M: うつ病は炎症性疾患であるが、細胞性免疫活性化がうつ病の鍵となる要素である。Prog Neuropsychopharmacol Biol Psychiatry 2011, 35:664-675.
- Howren MB, Lamkin DM, Suls J: うつ病とC反応性タンパク質・IL-1・IL-6の関連——メタ解析。Psychosom Med 2009, 71:171-186.
- Maes M, Lin AH, Delmeire L, Van Gastel A, Kenis G, De Jongh R, Bosmans E: 偶発的人為的外傷後PTSDにおける血清インターロイキン-6(IL-6)およびIL-6受容体濃度の上昇。Biol Psychiatry 1999, 45:833-839.
- Bonaccorso S, Puzella A, Marino V, Pasquini M, Biondi M, Artini M, Almerighi C, Levrero M, Egyed B, Bosmans E, Meltzer HY, Maes M: C型肝炎ウイルス患者へのIFNα免疫療法はサイトカインネットワークの相互連動した刺激と抑うつ・不安症状の増加を誘発する。Psychiatry Res 2001, 105:45-55.
- Wichers MC, Kenis G, Koek GH, Robaeys G, Nicolson NA, Maes M: IFNα誘発性の抑うつ症状はサイトカインネットワークの変化と関連しているがコルチゾールとは関連しない。J Psychosom Res 2007, 62:207-214.
- Anisman H: ストレッサーと炎症性免疫系活性化のカスケード効果——大うつ病性障害への示唆。J Psychiatry Neurosci 2009, 34:4-20.
- Piser TM: うつ病のサイトカイン仮説と神経回路仮説の連結——新規抗うつ薬の発見と開発のための翻訳的枠組み。Brain Behav Immun 2010, 24:515-524.
- Swiergiel AH, Dunn AJ: 高架式十字迷路とオープンフィールドテストにおけるマウスの行動に対するIL-1βとLPSの効果。Pharmacol Biochem Behav 2007, 86:651-659.
- Frenois F, Moreau M, O’Connor J, Lawson M, Micon C, Lestage J, Kelley KW, Dantzer R, Castanon N: LPSはマウスの拡大扁桃体・海馬・視床下部においてうつ病様行動の発現と並行する遅延FosB/ΔFosB免疫染色を誘発する。Psychoneuroendocrinol 2007, 32:516-531.
- Lacosta S, Merali Z, Anisman H: 急性・反復インターロイキン-2投与が空間学習・運動活性・探索行動・不安に及ぼす影響。Behav Neurosci 1999, 113:1030-1041.
- Song C, Phillips AG, Leonard B: インターロイキン1βはラットにおける条件性恐怖記憶を増強する——グルココルチコイドの関与の可能性。Eur J Neurosci 2003, 18:1739-1743.
- Nathan C: 炎症の制御点。Nature 2002, 420:846-852.
- Adib-Conquy M, Cavaillon JM: 補償的抗炎症応答症候群。Thromb Haemost 2009, 101:36-47.
- Tracey KJ: 炎症反射。Nature 2002, 420:853-859.(レビュー)
- Bone RC: 敗血症における重要な新知見。JAMA 1997, 278:249.
- Burdette SD, Parilo MA, Kaplan LJ, Bailey H: 全身性炎症反応症候群。Medscape, eMedicine 2010.
- Maes M, Meltzer HY, Scharpé S, Bosmans E, Suy E, De Meester I, Calabrese J, Cosyns P: うつ病における血漿L-トリプトファン低値と免疫炎症変数の関係。Psychiatry Res 1993, 49:151-165.
- Maes M, Scharpé S, Meltzer HY, Okayli G, Bosmans E, D’Hondt P, Vanden Bossche BV, Cosyns P: 大うつ病におけるネオプテリンとIFNγ分泌の増加と血漿L-トリプトファン利用可能性の低下——免疫応答のさらなる証拠。Psychiatry Res 1994, 54:143-160.
- Maes M, Leonard BE, Myint AM, Kubera M, Verkerk R: うつ病の新しい「5-HT」仮説——細胞性免疫活性化がIDOを誘発し、血漿トリプトファンの低下と有害なトリプトファン代謝産物(TRYCATs)の合成増加をもたらし、両者がうつ病発症に寄与する。Prog Neuropsychopharmacol Biol Psychiatry 2011, 35:702-721.
- Song C, Lin A, Bonaccorso S, Heide C, Verkerk R, Kenis G, Bosmans E, Scharpe S, Whelan A, Cosyns P, de Jongh R, Maes M: 原発性睡眠障害と大うつ病患者における炎症反応系と血漿トリプトファン利用可能性。J Affect Disord 1998, 49:211-219.
- Werner-Felmayer G, Werner ER, Fuchs D, Hausen A, Reibnegger G, Wachter H: TNFαとLPSはヒト細胞においてIFN誘発性トリプトファン分解とプテリジン合成を増強する。Biol Chem Hoppe Seyler 1989, 370:1063-1069.
- Takikawa O, Yoshida R, Yasui H, Hayaishi O: 肝外組織における血漿キヌレニンとIDO活性の関係。Progress in Tryptophan and Serotonin Research 所収。Berlin-New York: Walter de Gruyter and Co; 1984:517-520.
- Moroni F, Russi P, Gallo-Mezo MA, Moneti G, Pellicciari R: ラット脳におけるキノリン酸とキヌレン酸含量の調節——内毒素とニコチニルアラニンの効果。J Neurochem 1991, 57:1630-1635.
- Bonaccorso S, Marino V, Puzella A, Pasquini M, Biondi M, Artini M, Almerighi C, Verkerk R, Meltzer H, Maes M: C型肝炎受診患者においてIFNαベース免疫療法中に増加した抑うつ評価はIFNα誘発性セロトニン系の変化と関連する。J Clin Psychopharmacol 2002, 22:86-90.
- Maes M, Verkerk R, Bonaccorso S, Ombelet W, Bosmans E, Scharpé S: 産褥早期の抑うつ・不安症状はトリプトファンからキヌレニンへの分解増加と関連しており、これは免疫活性化と関連する現象である。Life Sci 2002, 71:1837-1848.
- Toker L, Amar S, Bersudsky Y, Benjamin J, Klein E: トリプトファン枯渇と気分障害の生物学。Isr J Psychiatry Relat Sci 2010, 47:46-55.
- O’Connor JC, André C, Wang Y, Lawson MA, Szegedi SS, Lestage J, Castanon N, Kelley KW, Dantzer R: BCG(カルメット・ゲラン桿菌)への応答においてIFNγとTNFαはマウスのミクログリアにおけるIDOのアップレギュレーションとうつ病様行動の誘発を媒介する。J Neurosci 2009, 29:4200-4209.
- Hoes MJ: 精神科患者における高キサンツレン酸排泄の臨床的意義。Acta Psychiatr Belg 1979, 79:638-646.
- Møller SE, Kirk L, Honoré P: 内因性うつ病におけるトリプトファン耐性と代謝。Psychopharmacology (Berl) 1982, 76:79-83.
- Maes M, De Ruyter M, Suy E: うつ病患者におけるL-トリプトファン負荷後の24時間尿中キサンツレン酸排泄。Acta Psychiatr Belg 1986, 86:120-130.
- Maes M, De Ruyter M, Suy E: うつ病患者におけるL-トリプトファン負荷後のキサンツレン酸の腎排泄。Hum Psychopharmacol Clin Exp 1987, 2:231-235.
- Myint AM, Kim YK, Verkerk R, Scharpé S, Steinbusch H, Leonard B: 大うつ病におけるキヌレニン経路——神経保護機能障害の証拠。J Affect Disord 2007, 98:143-151.
- Gabbay V, Klein RG, Katz Y, Mendoza S, Guttman LE, Alonso CM, Babb JS, Hirsch GS, Liebes L: メランコリー特徴を伴う青年期うつ病におけるキヌレニン経路の可能な役割。J Child Psychol Psychiatry 2010, 51:935-943.
- Steiner J, Walter M, Gos T, Guillemin GJ, Bernstein HG, Sarnyai Z, Mawrin C, Brisch R, Bielau H, Meyer zu Schwabedissen L, Bogerts B, Myint AM: 重症うつ病は前帯状回亜領域においてミクログリアのキノリン酸増加と関連する——免疫調節されたグルタミン酸作動性神経伝達の証拠? J Neuroinflammation 2011, 8:94.
- Sublette ME, Galfalvy HC, Fuchs D, Lapidus M, Grunebaum MF, Oquendo MA, Mann JJ, Postolache TT: 大うつ病における自殺企図者において血漿キヌレニンレベルが上昇している。Brain Behav Immun 2011, 25:1272-1278.
- Anderson G, Maes M, Berk M: うつ病・身体化・慢性疲労症候群の共通性の生物学的基盤。Med Hypotheses 2012, 78:752-756.
- Celik C, Erdem M, Cayci T, Ozdemir B, Ozgur Akgul E, Kurt YG, Yaman H, Isintas M, Ozgen F, Ozsahin A: 大うつ病における血清ネオプテリンレベルとうつ病エピソード数の関連。Prog Neuropsychopharmacol Biol Psychiatry 2010, 34:372-375.
- Maes M, Ombelet W, De Jongh R, Kenis G, Bosmans E: 分娩後の炎症応答は大うつ病の既往を持つ女性で増幅される——大うつ病は炎症反応系の感作を伴うことを示唆する。J Affect Disord 2001, 63:85-92.
- Liukkonen T, Silvennoinen-Kassinen S, Jokelainen J, Räsänen P, Leinonen M, Meyer-Rochow VB, Timonen M: C反応性タンパク質レベルとうつ病の関連——フィンランド北部1966年出生コホート研究の結果。Biol Psychiatry 2006, 60:825-830.
- Hennessy MB, Paik KD, Caraway JD, Schiml PA, Deak T: 母子分離中の炎症前活性とうつ病様行動の感作。Behav Neurosci 2011, 125:426-433.
- Kawasaki Y, Zhang L, Cheng JK, Ji RR: 中枢感作のサイトカインメカニズム——表在性脊髄における神経活性とシナプス活性の調節におけるIL-1β・IL-6・TNFαの独自かつ重複する役割。J Neurosci 2008, 28:5189-5194.
- Maes M, Ringel K, Kubera M, Berk M, Rybakowski J: 5-HTに対する自己免疫活性の増加——炎症・細胞性免疫活性化と関連し、うつ病の重症度とステージングと関連するうつ病の鍵となる要素。J Affect Disord 2012, 136:386-392.
- Hochstrasser T, Ullrich C, Sperner-Unterweger B, Humpel C: 炎症性刺激はセロトニン作動性ニューロンの生存を低下させ、ラット背側縫線核オルガノタイプ脳スライスにおいてIDOの神経発現を誘発する。Neuroscience 2011, 184:128-138.
- Maes M, Bosmans E, De Jongh R, Kenis G, Vandoolaeghe E, Neels H: 大うつ病と治療抵抗性うつ病における血清IL-6とIL-1受容体拮抗薬濃度の増加。Cytokine 1997, 9:853-858.
- Maes M, Vandoolaeghe E, Neels H, Demedts P, Wauters A, Meltzer HY, Altamura C, Desnyder R: 大うつ病における血清亜鉛低値は治療抵抗性と免疫・炎症応答の感受性マーカーである。Biol Psychiatry 1997, 42:349-358.
- Kubera M, Van Bockstaele D, Maes M: 治療抵抗性大うつ病における白血球サブセット。Pol J Pharmacol 1999, 51:547-549.
- O’Brien SM, Scully P, Fitzgerald P, Scott LV, Dinan TG: 選択的セロトニン再取り込み阻害薬療法に反応しないうつ病患者における血漿サイトカインプロファイル。J Psychiatr Res 2007, 41:326-331.
- Jacka FN, Maes M, Pasco JA, Williams LJ, Berk M: 女性における栄養素摂取と一般的精神障害。J Affect Disord(出版予定)。
- Maes M, Yirmyia R, Noraberg J, Brene S, Hibbeln J, Perini G, Kubera M, Bob P, Lerer B, Maj M: うつ病の炎症・神経変性(I&ND)仮説——将来の研究とうつ病における新薬開発への示唆。Metab Brain Dis 2009, 24:27-53.
- Maes M, Bosmans E, Calabrese J, Smith R, Meltzer HY: 統合失調症と躁病におけるIL-2とIL-6——抗精神病薬と気分安定薬の効果。J Psychiatr Res 1995, 29:141-152.
- Maes M, Delange J, Ranjan R, Meltzer HY, Desnyder R, Cooremans W, Scharpé S: 統合失調症・躁病・大うつ病における急性期タンパク質——向精神薬による調節。Psychiatry Res 1997, 66:1-11.
- Liu HC, Yang YY, Chou YM, Chen KP, Shen WW, Leu SJ: 双極性障害の急性躁病エピソードにおける免疫学的変数。J Neuroimmunol 2004, 150:116-122.
- Wadee AA, Kuschke RH, Wood LA, Berk M, Ichim L, Maes M: 急性躁病エピソードを持つ患者における血清学的観察。Hum Psychopharmacol 2002, 17:175-179.
- Maes M, Galecki P, Chang YS, Berk M: 大うつ病における酸化・窒素化ストレス(O&NS)経路と、その疾患における(神経)変性プロセスへの寄与の可能性についてのレビュー。Prog Neuropsychopharmacol Biol Psychiatry 2011, 35:676-692.
- Maes M, Mihaylova I, Leunis JC: 慢性疲労症候群(CFS)と大うつ病におけるホスファチジルイノシトール(Pi)に向けられた血清IgM抗体の増加——IgM介在性Pi免疫応答がCFSとうつ病両者の合併症の基盤となる一因子であるという証拠。Neuro Endocrinol Lett 2007, 28:861-867.
- Maes M, Mihaylova I, Kubera M, Leunis JC, Geffard M: うつ病における複数のネオエピトープに向けられたIgM介在性自己免疫応答——炎症性・神経進行性病態生理を支える新たな経路。J Affect Disord 2012, 135:414-418.
- Wichers MC, Koek GH, Robaeys G, Praamstra AJ, Maes M: 植物的症状の早期増加はIFNα誘発性認知・抑うつ変化を予測する。Psychol Med 2005, 35:433-441.
- Leonard BE, Myint A: 炎症とうつ病——認知症との因果関係はあるか。Neurotox Res 2006, 10:149-160.
- Song C, Wang H: サイトカインが動物モデルにおける炎症と神経新生の低下を媒介する。Prog Neuropsychopharmacol Biol Psychiatry 2011, 35:760-768.
- Catena-Dell’Osso M, Bellantuono C, Consoli G, Baroni S, Rotella F, Marazziti D: うつ病における炎症性・神経変性経路——抗うつ薬開発の新たな道。Curr Med Chem 2011, 18:245-255.
- Gorwood P, Corruble E, Falissard B, Goodwin GM: うつ病が脳機能に与える毒性効果——多数のうつ病外来患者における遅延再生の障害と累積うつ病期間。Am J Psychiatry 2008, 165:731-739.
- Lampe IK, Hulshoff Pol HE, Janssen J, Schnack HG, Kahn RS, Heeren TJ: 反復性大うつ病性障害を持つ女性患者における全脳灰白質体積減少とうつ病期間の関連。Am J Psychiatry 2003, 160:2052-2054.
- McKinnon MC, Yucel K, Nazarov A, MacQueen GM: 大うつ病性障害患者における海馬体積の臨床的予測因子を検討するメタ解析。J Psychiatry Neurosci 2009, 34:41-54.
- Videbech P, Ravnkilde B: 海馬体積とうつ病——MRI研究のメタ解析。Am J Psychiatry 2004, 161:1957-1966.
- MacQueen GM, Campbell S, McEwen BS, Macdonald K, Amano S, Joffe RT, Nahmias C, Young LT: 大うつ病における疾患経過・海馬機能・海馬体積。Proc Natl Acad Sci USA 2003, 100:1387-1392.
- Lacerda AL, Nicoletti MA, Brambilla P, Sassi RB, Mallinger AG, Frank E, Kupfer DJ, Keshavan MS, Soares JC: 大うつ病性障害における基底核のMRI解剖学的研究。Psychiatry Res 2003, 124:129-140.
- Stockmeier CA, Mahajan GJ, Konick LC, Overholser JC, Jurjus GJ, Meltzer HY, Uylings HB, Friedman L, Rajkowska G: 大うつ病における死後海馬の細胞変化。Biol Psychiatry 2004, 56:640-650.
- Drevets WC, Price JL, Furey ML: 気分障害における脳構造・機能異常——うつ病の神経回路モデルへの示唆。Brain Struct Funct 2008, 213:93-118.
- Harrison NA, Brydon L, Walker C, Gray MA, Steptoe A, Critchley HD: 炎症は前帯状回下部活性とメゾリンビック連絡の変化を通じて気分変化を引き起こす。Biol Psychiatry 2009, 66:407-414.
- Koenigs M, Grafman J: うつ病の機能的神経解剖学——腹内側前頭前野と背外側前頭前野の異なる役割。Behav Brain Res 2009, 201:239-243.
- Park S-M, Gaykema RPA, Goehler LE: 免疫的挑戦はどのようにして嗜好性食物の摂取を阻害するか——全身性LPSが摂食神経回路の主要な節点を調節する。Brain Behav Immun 2008, 22:1160-1172.
- Kauer-Sant’Anna M, Kapczinski F, Andreazza AC, Bond DJ, Lam RW, Young LT, Yatham LN: 早期・後期ステージの双極性障害患者における脳由来神経栄養因子と炎症マーカー。Int J Neuropsychopharmacol 2009, 12:447-458.
- Jancsár SM, Leonard BE: 嗅球摘出ラットの条件性味覚嫌悪学習に対する抗うつ薬の効果。Neuropharmacology 1981, 20:1341-1345.
- Kumar RK, Wakefield D: 炎症:慢性。eLS 2010.
- Straub RH: 進化医学と慢性炎症状態——病態生理における既知と新知見。J Mol Med (Berl) 2012, 90:523-534.
- Jewkes RK, Dunkle K, Nduna M, Jama PN, Puren A: 南アフリカ農村部の若者における幼少期の逆境とうつ病・物質乱用・HIV・HSV2新規感染の関連。Child Abuse Negl 2010, 34:833-841.
- Pearce BD, Kruszon-Moran D, Jones JL: 第3回全米健康・栄養調査におけるToxoplasma gondii感染と気分障害の関係。Biol Psychiatry(出版予定)。
- Maes M: 興味深くも未解明の共起現象——うつ病と慢性疲労症候群は共通の炎症性・酸化的・窒素化的(IO&NS)経路の発現である。Prog Neuropsychopharmacol Biol Psychiatry 2011, 35:784-794.
- Owe-Larsson B, Säll L, Salamon E, Allgulander C: HIV感染と精神疾患。Afr J Psychiatry 2009, 12:115-128.
- Maes M, Kubera M, Leunis JC, Berk M: 慢性うつ病における腸内常在菌に対するIgAとIgM応答の増加——細菌トランスロケーション増加または腸管リーキーのさらなる証拠。J Affect Disord(出版予定)。
- Hassett AL, Radvanski DC, Buyske S, Savage SV, Sigal LH: 「慢性ライム病」患者における精神医学的合併症とその他の心理的要因。Am J Med 2009, 122:843-850.
- Strijdom SC, Berk M: 南アフリカにおけるライム病。S Afr Med J 1996, 86(Suppl):741-744.
- van den Pol AN: 脳機能障害につながるウイルス感染——一般に評価されているよりも頻繁か。Neuron 2009, 64:17-20.
- Maes M, Song C, Lin A, DeJong R, Van Gastel A, Kenis G, Bosmans E, DeMeester I, Neels H, Janca A, Scharpe S, Smith RS: 心理的ストレス誘発性IFNγとIL-10産生の免疫学的・臨床的相関。Cytokines, Stress and Immunity 所収、Plotnikoff NP 他編。New York: Taylor and Francis; 1998:39-50.
- Wohleb ES, Hanke ML, Corona AW, Powell ND, Stiner LM, Bailey MT, Nelson RJ, Godbout JP, Sheridan JF: β-アドレナリン受容体拮抗薬は反復社会的敗北によって誘発される不安様行動とミクログリア反応性を防ぐ。J Neurosci 2011, 31:6277-6288.
- Williams LJ, Pasco JA, Jacka FN, Henry MJ, Dodd S, Berk M: うつ病と骨代謝——レビュー。Psychother Psychosom 2009, 78:16-25.
- Pavlovićc Z, Delićc D, Marićc NP, Vukovićc O, Jašovićc-Gašićc M: ペグ化IFNα療法で治療されたC型肝炎患者における抑うつ症状——24週間前向き研究。Psychiatr Danub 2011, 23:370-377.
- Wichers MC, Koek GH, Robaeys G, Verkerk R, Scharpé S, Maes M: IDOとIFNα誘発性抑うつ症状——トリプトファン枯渇から神経毒性への仮説の転換。Mol Psychiatry 2005, 10:538-544.
- Kendler KS, Thornton LM, Gardner CO: 大うつ病発症予測における遺伝的リスク・過去のうつ病エピソード数・ストレスフルな生活上の出来事。Am J Psychiatry 2001, 158:582-586.
- Laugeray A, Launay JM, Callebert J, Surget A, Belzung C, Barone PR: マウスにおける不安・うつ様行動の調節における末梢キヌレニン経路の鍵となる役割の証拠——個体差への焦点。Pharmacol Biochem Behav 2011, 98:161-168.
- Wrynn AS, Mac Sweeney CP, Franconi F, Lemaire L, Pouliquen D, Herlidou S, Leonard BE, Gandon J, de Certaines JD: うつ病の嗅球摘出ラットモデルのin vivo MRI研究。Brain Res 2000, 879:193-199.
- Wang D, Noda Y, Tsunekawa H, Zhou Y, Miyazaki M, Senzaki K, Nabeshima T: 不安を伴ううつ病に類似した嗅球摘出ラットの行動・神経化学的特徴。Behav Brain Res 2007, 178:262-273.
- Huang Y, Henry CJ, Dantzer R, Johnson RW, Godbout JP: 脳室内LPSに応答した老齢マウスにおける病時行動の誇張と脳炎症性サイトカイン発現。Neurobiol Aging 2008, 29:1744-1753.
- Nakanishi H, Hayashi Y, Wu Z: 加齢依存性に延長したLPS誘発性病時行動におけるミクログリアのmtDNA損傷の役割。Neuron Glia Biol 2011, 28:1-7.
- Taepavarapruk P, Song C: アセチルコリン遊離と神経成長因子発現の低下はIL-1β投与によって誘発される記憶障害と相関する——ω3脂肪酸EPA治療の効果。J Neurochem 2010, 112:1054-1064.
- Lai AY, Swayze RD, El-Husseini A, Song C: IL-1βは海馬ニューロンにおけるAMPA受容体の発現とリン酸化を調節する。J Neuroimmunol 2006, 175:97-106.
- Kinney DK, Tanaka M: うつ病とその症状・適応価・リスク因子の進化的仮説。J Nerv Ment Dis 1980, 97:561-567.
- Raison CL, Miller AH: 病原体宿主防御(PATHOS-D)におけるうつ病の進化的意義。Mol Psychiatr 2012.
- Olde Hartman TC, Borghuis MS, Lucassen PL, van de Laar FA, Speckens AE, van Weel C: 医学的に説明できない症状・身体化障害・心気症——経過と予後。系統的レビュー。J Psychosom Res 2009, 66:363-377.
- Xia Z, DePierre JW, Nassberger L: 三環系抗うつ薬はヒト血液単球においてIL-6・IL-1β・TNFα放出を、T細胞においてIL-2とIFNγを阻害する。Immunopharmacology 1996, 34:27-37.
- Maes M, Song C, Lin AH, Bonaccorso S, Kenis G, De Jongh R, Bosmans E, Scharpe S: 抗うつ薬の負の免疫調節効果——IFNγ分泌の阻害とIL-10分泌の刺激。Neuropsychopharmacol 1999, 20:370-379.
- Brustolim D, Ribeiro-dos-Santos R, Kast RE, Altschuler EL, Soares MB: 抗炎症治療に新たな章が開く——抗うつ薬ブプロピオンはマウスにおけるTNFαとIFNγの産生を低下させる。Int Immunopharmacol 2006, 6:903-907.
- Castanon N, Bluthé RM, Dantzer R: 非定型抗うつ薬チアネプチンの慢性投与は、ラットにおける末梢投与のLPSとIL-1βによって誘発される病時行動を減弱させるが、中枢投与では減弱させない。Psychopharmacology (Berl) 2001, 154:50-60.
- Jiang Y, Deacon R, Anthony DC, Campbell SJ: 末梢TNF阻害はCNS炎症性疾患に関連する倦怠感を遮断しうる。Neurobiol Dis 2008, 632:125-132.
- Maes M, Meltzer HY, Bosmans E, Bergmans R, Vandoolaeghe E, Ranjan R, Desnyder R: 大うつ病における血漿IL-6・可溶性IL-6・可溶性IL-2・トランスフェリン受容体濃度の増加。J Affect Disord 1995, 34:301-309.
- Maes M, Fišar Z, Medina M, Scapagnini G, Nowak G, Berk M: うつ病における新たな薬物標的——炎症性・細胞性免疫・酸化および窒素化ストレス・ミトコンドリア・抗酸化・神経進行性経路。および新たな薬物候補——Nrf2活性化薬とGSK-3阻害薬。Inflammopharmacology 2012, 20:127-150.
- Hannestad J, DellaGioia N, Bloch M: 抗うつ薬治療が血清炎症性サイトカインレベルに与える効果——メタ解析。Neuropsychopharmacology 2011, 36:2452-2459.
- Kirsch I: 抗うつ薬とプラセボ応答。Epidemiol Psichiatr Soc 2009, 18:318-322.
- Tuma T: 4.5年後の入院治療うつ病の転帰——高齢コホートと若年コホートの比較。Br J Psychiatry 2000, 176:224-228.
- Twenge JM, Gentile B, DeWall CN, Ma D, Lacefield K, Schurtz DR: 若いアメリカ人における出生コホート別の精神病理増加、1938〜2007年——MMPIの通時的メタ解析。Clin Psychol Rev 2010, 30:145-154.

